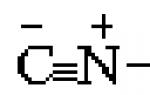Манган в кръвта
Определяне на концентрацията на манган в кръвта, използвана за диагностициране на остра и хронична манганова интоксикация, както и за оценка на баланса на този микроелемент в организма.
Синоними руски
Серумен манган.
Английски синоними
Mn, манган, серум.
Изследователски метод
Атомно -адсорбционна спектрометрия (AAS).
Единици
Mkg / L (микрограма на литър).
Какъв биоматериал може да се използва за изследване?
Венозна кръв.
Как правилно да се подготвим за изследването?
- Не яжте 2-3 часа преди изследването, можете да пиете чиста негазирана вода.
- Не пушете 30 минути преди изследването.
Обща информация за изследването
Манганът е елемент, открит в свободна форма в живата природа, както и в някои органични и неорганични съединения на човешкото тяло. Той е необходим за образуването на костна тъкан, синтеза на протеини, молекули АТФ и регулиране на клетъчния метаболизъм. В допълнение, манганът действа като кофактор на една от разновидностите на супероксид дисмутаза (манган), която неутрализира свободните радикали и ензимите на глюконеогенезата.
Този микроелемент влиза в тялото заедно с храната. Той присъства в големи количества в лешници, орехи, фъстъци, спанак, цвекло, чесън, кайсии и някои други храни. Дневното изискване на възрастен за манган е 1,8-2,6 mg. Обикновено само 1-3% от мангана, доставен с храната, се абсорбира в червата, докато по-голямата част от него се екскретира с изпражненията. Както в случая с други микроелементи, концентрацията на манган се поддържа на много ниско ниво, но достатъчно, за да се осигурят физиологични функции. Нарушенията на нейния баланс могат да бъдат остри или хронични и се диагностицират с помощта на кръвен манганов тест.
Хранителното отравяне с манганови соли е изключително рядко, тъй като обикновено само малка част от него се абсорбира в червата. По -голямата част от случаите на отравяне са примери за хронична интоксикация, свързана с вдишване на манганов прах. Най -застрашени са работниците в добива на руда и стоманодобива. Обширната повърхност на белите дробове осигурява бързо усвояване на мангана в кръвта, откъдето постъпва в различни органи. Отлагането на манган в мозъчната тъкан е придружено от развитието на характерен клиничен синдром, наречен манганов паркинсонизъм. Признаците включват нарушение на походката, лице, подобно на маска, дистония и лигавене. За разлика от идиопатичния паркинсонизъм, в тази форма няма тремор в покой, но могат да се наблюдават постурални и умишлени тремори. Диференциалната диагноза на идиопатичен и манганов паркинсонизъм е задължителна, тъй като болестите имат различна прогноза и се лекуват по различен начин. Особеността на мангановия паркинсонизъм е в липсата на отговор на лечение с допаминови препарати и в необратимостта на промените. Анализът на манган в кръвта дава възможност да се разграничат тези две състояния.
Също така може да се наложи оценка на нивото на манган в кръвта при преглед на млад пациент с признаци на атипичен паркинсонизъм. Някои хора, които използват и независимо произвеждат инжекционни лекарства, използват калиев перманганат като окислител, който навлиза в кръвта заедно с лекарството. В резултат на това концентрацията на манган при такива пациенти може да бъде 2000-3000 mg / l (за сравнение, нормата е 10-12 mg / l). Постоянното повишаване на нивата на манган уврежда невроните на субстанцията нигра на средния мозък, което води до характерни симптоми. Клиничната картина на манганов паркинсонизъм може да се наблюдава и при пациенти с чернодробни заболявания - той е основният орган, който осигурява екскрецията на манган от организма. При цироза на черния дроб отделянето на този елемент е трудно, в резултат на което той се натрупва в кръвта и мозъчната тъкан.
Смята се, че поради някои физиологични характеристики децата са изложени на по -голям риск от ентерално и инхалационно отравяне с манган. Така например, използването на вода с повишена концентрация на манганови соли е по -важно за развитието на болестта при децата, отколкото при възрастните. В допълнение, клиничните прояви на хронична манганова интоксикация при деца също се различават от тези при възрастни. Манганът има отрицателен ефект върху предаването на нервните импулси по допаминергичните пътища, които осигуряват внимание, координация и познавателна дейност. Поради това е препоръчително да се измерва нивото на кръвта му при преглед на дете с разстройство на хиперактивност с дефицит на внимание и увреждания при учене.
Вдишването на манганови пари също може да доведе до развитие на т. Нар. Метална треска. Това състояние се развива 3-12 часа след вдишване на пари от манганов оксид и е по-често при заварчици. Клиничната картина на заболяването прилича на грип: треска, кашлица, възпалено гърло, запушване на носа, задух, слабост, миалгия. Особеността на "металната треска" е, че всички симптоми изчезват след прекратяване на контакта с метални пари (например през уикендите). При изследване на кръв при такива пациенти понякога е възможно да се установи повишаване на концентрацията на манган. Трябва да се отбележи, че симптомите на "метална треска" не са специфични за остро отравяне с манган и се наблюдават и при вдишване на пари от цинков оксид, мед, желязо, олово и други метали. По този начин анализът за манган, както и за други метали в кръвта, може да се използва при диагностицирането на професионални заболявания.
Някои редки вродени метаболитни заболявания са придружени от дефицит на манган. По -често липсата му се проявява при пациенти, които са били на парентерално хранене дълго време. Признаци на дефицит на манган: нарушен растеж и минерализация на костите, метаболизъм на въглехидрати и мазнини. Измерването на концентрацията на манган в кръвта на такива пациенти е необходимо за оценка на баланса на този микроелемент в организма.
За какво се използват изследванията?
- За диагнозата "метална треска" при заварчика.
- За диагностика на манганов паркинсонизъм при минни работници, млади хора, инжектиращи наркотици, и пациенти с цироза.
- За диагностика на хронична манганова интоксикация при деца с разстройство на дефицит на вниманието, при хиперактивни деца и деца с увреждания в ученето.
- За оценка на баланса на мангана в организма при пациент на пълно парентерално хранене.
Кога е насрочено изследването?
- Със симптоми:
- паркинсонизъм, особено при минни работници, млади хора, които инжектират наркотици, и пациенти с цироза на черния дроб (нарушения на походката и баланса, лице, подобно на маска, дистония, постурален и умишлен тремор);
- грипоподобен синдром при заварчици (треска, кашлица, възпалено гърло, запушване на носа, задух, слабост, миалгия);
- разстройство на хиперактивност с дефицит на внимание при деца (невъзможност за концентрация, лесно отвличане на вниманието към външни стимули - играчки, прибори за писане, - невъзможност да завършат упражненията до края, да изчакат своя ред в игрите, да се намесват в разговор, да вика от място).
- При наблюдение на пациент на пълно парентерално хранене.
Какво означават резултатите?
Референтни стойности: 0 - 2 μg / L.
Причини за повишаване нивото на манган в кръвта:
- остро или хронично отравяне с манган;
- цироза на черния дроб.
Изобилието от манган е доста високо; той се нарежда на 14 -то място сред най -разпространените минерали. Налице е в много продукти и естествено във вода, тъй като се разтваря перфектно. И като всеки елемент, който влиза в храната, той може да бъде полезен или вреден. Така че пречистването на водата от манган и поддържането й в задоволителен стандарт е от голямо значение. 
ГОСТ: манган в питейна вода
- в централизирани системи - ≤ 0,1 mg / l;
- манган във вода от кладенци и други открити източници - ≤ 0,5 mg / l.
В природата манганът може да образува до 8 вида оксиди, от MnO до Mn5O8 и се намира в медни и железни руди. Образуването на оксиди зависи от състава на средата и външните физични параметри. Най -стабилният оксид - MnO2, който е и най -разпространеният в недрата на земята, се нарича пиролузит. 
Поради широкото използване на минерала в металургията и химическото производство, специално внимание се обръща на съдържанието му в промишлените отпадъци. Количеството манган в отпадъчните води не трябва да надвишава 0,01 mg / dm3.
Манган във вода: въздействие върху тялото и визуално определяне на неговото присъствие
Както знаете от медицинската практика, дори малко количество отровно вещество може да има благоприятен ефект върху организма, но превишаването на неговата норма ще доведе до непоправими последици.
Полезни функции на мангана в организма
В зависимост от възрастта, допустимите дневни дози варират и са:

Манганът може да се получи както от вода, така и от храна. На територията на Русия няма райони с ниско съдържание на Mn; дори има излишък от манган във водата. Участието на минерала във физиологичните процеси на живите организми е незаменимо. Основните му функции са:
- коригиране на нивата на глюкоза, стимулиране на синтеза на аскорбинова киселина;
- ограничаване развитието на диабет;
- подпомагане дейността на нервната система и мозъка;
- производство на холестерол и подпомагане функционирането на панкреаса;
- образуването на съединителна, хрущялна и костна тъкан;
- регулиране на липидния метаболизъм и предотвратяване на затлъстяването на черния дроб;
- участие в клетъчното делене и обновяване;
- ограничаване на активността на холестерола и предотвратяване на растежа на плаки;
- активиране на ензими за усвояване на витамините В1, С и биотин от организма.
Може да се използва като антиоксидант при взаимодействие с Fe и Cu. Манганът се задържа в организма от Р и Са. Яденето на храна с високо съдържание на въглехидрати води до бързото елиминиране на Mn резервите в организма. Количеството манган във водата може да има както положителни, така и отрицателни ефекти. При някои условия се образува дефицит на манган, нормата във водата не покрива дневните му нужди за кърмещи майки и спортисти.
Вреда от излишък на манган във вода
След това манганът във вода е опасен за физиологичните функции, намалява абсорбцията на желязо и се конкурира с медта, а това е анемия и сънливост. Значителна вреда е нанесена на централната нервна система, която се изразява в намаляване на работоспособността и развитие на ранна амнезия. Тежкият метал Mn може да увреди белите дробове, черния дроб и сърцето в големи дози и да спре лактацията при кърмещи жени.
Здравето, един от основните стремежи на човек, но ежедневните проблеми, създавани от манганови съединения, могат да дразнят много. Визуално определяне на манган в питейна вода се извършва чрез проверка на водопроводни инсталации и прибори, които са били в контакт с течност от чешмата дълго време. 
Най -често минералът придружава черното желязо и образува с него неразтворими съединения. Черни отлагания се образуват върху водопроводни инсталации, прибори за храна, котлен камък се натрупва бързо в електрическите уреди и пропускливостта на тръбите намалява. Твърде високо ниво на замърсяване, това вече се вижда при изтегляне на вода от чешмата и дори вкусва и мирише. В тези случаи е необходимо незабавно да се анализира водата, манганът и желязото трябва да бъдат основните изследвани параметри в нея.
Пречистване на водата от желязо и манган
Във чешмяна или артезианска вода минералът е под формата на двувалентен положителен йон (Mn2 +), който се разтваря добре в течности. За да се отстрани манганът от водата, той се превръща в неразтворими форми - три или четиривалентни. Плътната утайка се отстранява с гранулирани каталитични среди или йонообменни смоли.
Манганови филтри и методи за филтриране

Методи, използвани при деманганиране:
Проветряване.Използва се при наличие на желязо във водата. Под действието на аериране желязото се окислява и превръща в хидроксид. Полученото съединение свързва двувалентен манган и го утаява. Твърдите примеси се филтрират през кварцов пясък.
Каталитично окисляване.Извършва се с 4-валентен манганов хидроксид.
Окисляващи реактиви.Тук се използват озон, натриев хипохлорит, самият хлор и неговият диоксид.
Йонна обмяна.Извършва се в два вида смоли: анионообменна (OH–) и катионообменна (H +).
Дестилация.Въз основа на разликата в точките на кипене между водата и нейните примеси. След процедурата е необходима минерализация на водата.
В зависимост от резултатите от анализа за обема на манган във водата се избира филтър със специфичен метод на филтриране. Или допълнително пречистване на водата се извършва чрез комплекс от филтриращи компоненти, които постоянно намаляват замърсяването на течността.
Манганът е елемент от страничната подгрупа на седмата група от четвъртия период на периодичната система от химични елементи на Д. И. Менделеев, атомен номер 25. Обозначен е със символа Mn.
Манганът е един от най -често срещаните елементи, съставлявайки 0,03% от общия брой атоми в земната кора. Сред тежките метали (атомно тегло над 40) манганът е на трето място по разпределение в земната кора, след желязото и титана.
Манганът е много интересен биохимично. Точните анализи показват, че той присъства в организмите на всички растения и животни. Съдържанието му обикновено не надвишава хилядни от процента, но понякога е много по -високо. Например листата от цвекло съдържат до 0,03%, в тялото на червените мравки - до 0,05%, а при някои бактерии дори до няколко процента манган.
Манганът е един от малкото елементи, които могат да съществуват в осем различни окислителни състояния. Само две от тези състояния се реализират в биологичните системи: Mn (II) и Mn (III).
Манганът присъства в естествените води в различни форми, които зависят от киселинността на околната среда. В подземните води, при липса на кислород, манганът обикновено се намира под формата на двувалентни соли. В повърхностните води манганът е под формата на органични комплексни съединения, колоиди и фини суспендирани вещества.
Основните източници на манганови съединения са:
1. Питейната вода е източник на прием на манган, тъй като стандартите за пречистени отпадъчни води за изпускане в залива са 10 пъти по -строги от стандартите за питейна вода (действителното съдържание на манган в питейната вода е до 0,05 mg / dm 3).
2. Подземни води (съдържание на манган до 0,5 mg / dm 3): в случай на оттичане в гравитачната канализационна система.
3. Външни абонати: предприятия с независими източници на водоснабдяване (кладенци) (съдържание на манган до 0,1 mg / dm 3), фекална вода от цистерни (съдържание на манган до 0,6 mg / dm 3).
В резултат на това откриваме, че концентрацията на общия манган на входа на битовите съоръжения за пречистване на отпадъчни води е 0,3 - 0,4 mg / dm 3.
Съдържанието на манган в повърхностните водни обекти е променливо и има изразени периодични колебания. Максимумите се наблюдават през зимно-пролетния период (пик февруари-март), летния период (пикът август) и есенно-зимния период. През тези периоди съдържанието на манган в повърхностните водни обекти може да бъде десетки пъти по -високо от средните стойности. Възможни причини за пика февруари-март: намаляване на концентрацията на разтворен кислород и рН на водата (с все още съществуващата ледена покривка), намаляване на ролята на окислителните процеси във водния стълб. Увеличаването на концентрацията на свободен манган през август се улеснява от: смъртта на фитопланктон, по-специално синьо-зелени водорасли, които отделят манган под формата на свободни катиони Mn (II) (около 60%) и нискомолекулни съединения ( около 30-35%), намаляване на концентрацията на разтворен кислород, който се изразходва за окисляване на "органичната материя" на разлагащите се водни организми. Трябва да се отбележи, че разлагането на висша водна растителност, последвано от отделянето на Mn (II) във водата, продължава в рамките на 7-8 месеца. Това обстоятелство очевидно може да бъде замесено и във връх февруари-март.
Високите концентрации на разтворен манган през есенно-зимния период се дължат на приемането му от тинести води. Този период е много близо през зимата и пролетта. При редуциращи условия съдържанието на разтворени форми на манган във водите от утайки е 1-3 mg / dm 3.
Невротоксичността на мангана не е напълно изяснена. Има доказателства, че манганът взаимодейства с желязо, цинк, алуминий и мед. Въз основа на редица проучвания, нарушеният метаболизъм на желязото се счита за възможен механизъм на увреждане на нервната система. Това може да доведе до окислително увреждане.
Възможно е дългосрочното натрупване на манган да повлияе на способността за възпроизвеждане. В проучвания при животни, бременността при продължително излагане на високи дози манган е по -вероятно да доведе до вродени малформации при потомството.
Манганът може да попречи на чернодробната функция, но експериментите показват, че прагът на токсичност е много висок. От друга страна, повече от 95% манган се екскретира от тялото в жлъчката и всяко увреждане на черния дроб може да забави детоксикацията чрез увеличаване на концентрацията на манган в кръвната плазма.
Тези обстоятелства свидетелстват в полза на затягане на стандартите за съдържанието на соли на този тежък метал в отпадъчните води.
Mamchenko A.V., Kiy N.N., Yakupova I.V., Chernova L.G., Deshko I.I.,
Институт по колоидна химия и химия на водата на Националната академия на науките на Украйна, Киев
Антропогенната човешка дейност и непрекъснатото увеличаване на мащаба на потреблението на вода доведоха до качествено влошаване на източниците на сладка вода (1, 2). Мониторингът на екологичното състояние на естествените води (2-14) показа многократно превишаване на екологичния оптимум във водите на повечето страни - повсеместното присъствие на съединения на желязо, манган, амоний, флуор във водите на Франция (5), RF (6-9, 12, 13), Китай (14), натрупване на големи количества манган в Кременчугските и низходящите водоеми на Украйна (11), надвишаващи три пъти екологичния оптимум за речния басейн. Припят (4) (Украйна и Беларус) и др.
Влошаването на качеството на повърхностните източници ни принуди да се обърнем към подземните води, чийто състав е по -стабилен, не подлежи на сезонни колебания и влиянието на повърхностното замърсяване в околните райони и не съдържа най -трудните замърсители от точката на изглед на пречистване на водата - органични вещества, тежки метали, бактерии, вируси.
В повечето случаи обаче подземните води поради незадоволителни геохимични условия на образуване (в земната кора съдържанието на манган е около 0,1%) са нестандартни за пиене. Въпреки значителния почистващ ефект от филтрирането през почвата, водата, взета от артезиански кладенци, често има повишено съдържание на желязо, манган и соли на твърдост. Същевременно се наблюдава устойчива тенденция към увеличаване на концентрацията им и надвишаване на ПДК за питейна вода. Опасността от замърсяване на подземните води с манган, желязо и други метали идва от разработването на рудни находища и експлоатацията на открити ями (6,8,9,15). Съществуващите технологии само частично решават този проблем (16, 17).
Съгласно нормативните препоръки на СЗО и SANPiN (18, 19), максимално допустимата концентрация на манган в питейна вода е 0,1 mg / dm 3; желязо - 0,3 mg / dm 3. Изискванията на много индустрии: храна, енергия, електроника, са много по -строги (18, 20).
Нуждата на човешкото тяло от манган се осигурява, като правило, от съдържанието му във вода и храна. Дневният прием на манган от храната е средно 3,7 (от 2,2 до 9) mg, от въздуха - 0,002 mg, от питейната вода - до 0,064 mg (21). Дефицитът на манган в човешкото тяло води до нарушения във функционирането на репродуктивната, нервната и слуховата система и нарушения в скелетната формация (22).
Превишаването на нормата има мутагенен ефект върху човек. Притежавайки изразени кумулативни свойства, манганът се натрупва в черния дроб, бъбреците, мозъка, щитовидната жлеза и панкреаса и лимфните възли. В стратегията за управление на риска питейната вода, макар и незначителен източник на прием на манган, трябва да се разглежда заедно с други потенциални източници на излагане на хора. Установена е тясна връзка между високото съдържание на манган в питейната вода и храната и невротоксикацията при малки деца (23-25) и металурзите (26), състояние, известно като "манганизъм" и в много отношения подобно на болестта на Паркинсон (27 -29), неврологични прояви при жителите на индустриалните райони на Гърция (30), психични разстройства, мускулни тремори при жители на Япония (31) и др.
Следователно използването на подземни води с високо съдържание на манган и други примеси е възможно само ако има ефективни технологии за пречистване от тях.
Процесът на деманганиране -обезвъздушаване се определя от природата на манганови и железни съединения - минерални или органични; рН, концентрация на свободен въглероден диоксид, разтворен кислород, редокс потенциал, сулфиди, органични вещества, твърдост, обща минерализация, разтворени газове (32-35).
Във водата манганът се намира в три дисперсионни области: молекулярна, колоидна и гравиметрична. Молекулни дисперсии (d<1 ммк) не осаждаются, проходят через все фильтры, диализируют и диффундируют. Коллоидные системы – гидрофобные золи проходят сквозь фильтры тонкой чистки, но задерживаются фильтрами сверхтонкой очистки, заметно не осаждаются, не диализируют и весьма незначительно диффундируют, видны в ультрамикроскоп. Простые дисперсии или суспензии (d>100 mmk) се утаяват след известно време, не са способни на диализа и дифузия, не преминават през фини хартиени филтри. Съединенията на манган и желязо от колоидни дисперсии се трансформират в суспензии поради коагулация на мицели (33).
Наличието на манган във вода се дължи на разтворимостта на образуваните от него съединения. При рН 4-7,5, йоните Mn 2+ доминират във вода, в случай на високи стойности на редокс потенциала, утайка от манганов диоксид; при рН> 7,5, манганът се отделя под формата на хидроксид или оксиди на различни валентности (35, 36). Разтворимостта на Mn (II) може да контролира равновесието на манганов оксид с манган в други окислителни състояния. В силно редуцираща среда съдържанието на манган зависи от образуването на слабо разтворими сулфиди (37). Хуминовите съединения определят колоидното състояние (10, 11, 36) и стабилни, трудно окисляващи се органични манганови комплекси.
В източниците на повърхностни води, при естествени условия, е възможно фотокаталитично редуциране с образуване на йони на Mn 2+ и ускоряване на окислителните реакции поради участието на манган в процесите на фотосинтеза по време на възпроизвеждането на водорасли, което намалява концентрацията му във вода ( 38).
В подземните води манганът най-често се намира в силно разтворима форма на бикарбонат (0,5-4 mg / dm 3) или хидроксид, много по-рядко под формата на манганов сулфат. (10, 35). Той може да образува комплекси с фосфатни йони и някои органични лиганди (11). В подземните води с ниско съдържание на кислород Mn (II) се окислява химически или биологично до Mn (IV) (37). Манганът обикновено се намира във вода, съдържаща желязо. Химически може да се счита за сроден на жлезата, защото те имат същата структура на външния електронен слой.
Разнообразието от фактори, които определят състава на естествените води и тяхната променливост изключват възможността за разработване на единен универсален икономически обоснован метод, приложим във всички случаи на живот. Практически се използва цялата гама от технологии за пречистване на вода, разработени до момента. Често при избора на технология за конкретен водоизточник се комбинират няколко метода, тъй като всеки от тях има както предимства, така и недостатъци.
Отстраняването на желязо и манган често се решава в рамките на единна технология, като се отчита спецификата на извличането на всеки компонент (33). Двувалентните железни и манганови йони се окисляват съответно до тривалентно и четиривалентно състояние, реакционните продукти се отделят от течната фаза (чрез коагулация на колоидни съединения и задържане в резервоари за утаяване или на филтри в резултат на адсорбция, хемосорбция или каталитично окисляване явления) (29, 39-41). Натрошен базалт и базалтов чакъл (2), кварцов пясък, доломит, калциев карбонат, мрамор, манганов (IV) оксид, антрацит, полимерни материали (35) се използват като филтриращ материал.
Окисляването на разтворимия Mn (II) с кислород протича много по -бавно от разтворимия Fe (II). Mn (II) не може да се окисли чрез просто аериране на водата. За да се ускори процесът, се използват специални гранулирани каталитични фуражи, върху които настъпва окисляване с едновременното отделяне на окислени вещества (42-46).
Окислението без реагенти с кислород на въздуха чрез вакуумно изхвърляне (47) или дълбоко аериране (29, 39), под високо налягане (48), изкуственото окисляване с кислород (49, 50) на подземните води води до отстраняване на CO 2, H 2 S, CH 4 от него, променят околната среда от редуцираща до окисляваща, увеличавайки редокс потенциала до 250-500 mV и рН до 7 или повече. Образува се слой от Fe (OH) 3, чиято повърхност абсорбира Fe (II) и Mn (II) йони и молекулен кислород. Последният при нормални условия окислява разтворените желязо и манганови йони до слабо разтворими железни и манганови оксихидрати, които лесно се отделят чрез филтриране. Когато манганов диоксид или друго каталитично активно вещество се добави към пясъчен филтър, въздухът, разтворен във вода, осигурява каталитично окисляване и утаяване на манган (51).
По време на окисляване с въздушен кислород съгласно метода Viredox, разработен от финландска компания, около 10% от общия дебит на водата, наситена с въздушен кислород, се изпомпва обратно във водоносния хоризонт през няколко абсорбционни кладенци, разположени в кръг с радиус 5- 10 м около добивния кладенец (52, 53). В резултат на биохимични и химични процеси манганът се трансформира в неразтворима форма и се утаява във водоносния хоризонт. Въпреки това, с простотата и рентабилността на метода, той не винаги гарантира правилната степен на пречистване на водата от манган и създава опасност от запушване на водоносния хоризонт. Очевидно този метод може да се приложи само ако има хидрогеоложка обосновка. Това беше направено за подземните води в залива Консепсион и прилежащия континентален шелф (54), като методът осигури подходяща дълбочина на деманганиране.
Химическото окисляване се извършва с хлор и неговите производни, озон, калиев перманганат и др.
С помощта на хлор се отстраняват желязото и манганът, сероводородът се унищожава и обезцветява (оптимално рН> 4) (55-57), съчетавайки в определени случаи почистване с дезинфекция (рН 8) (57). Съществени недостатъци на газообразния хлор се считат за повишените изисквания за безопасност при транспортирането и съхранението му и потенциалния риск за здравето, свързан с образуването на трихалометани (THM): хлороформ, дихлорбромометан, дибромохлорометан и бромоформ (58). Използването на натриев или калциев хипохлорит вместо молекулен хлор не намалява, но значително увеличава вероятността от образуване на THM (55, 59).
Известната технология за деманганиране на вода, която използва комбинираното действие на дълбоко аериране и хлор, което действа като окислител и като катализатор за окислителното действие на разтворения кислород (20).
Най-мощният от известните естествени окислители е озонът, който не образува хлор-съдържащи трихалометани (60, 61) и окислява Mn (II) при рН 6,5-7,0 за 10-15 минути (30, 62, 63).
Озонът обаче е нестабилно химично съединение с много висока химическа активност, което образува странични продукти (алдехиди, кетони, органични киселини, бромосъдържащи трихалометани, бромати, пероксиди, бромооцетна киселина). За отстраняване на страничните продукти са необходими допълнителни филтри и следователно високи първоначални разходи за оборудване и последващи такива - за поддръжка на завода (64). Изследванията за определяне на ефективността на пречистването на водата от Mn (II) от Mn (II) в река Днепър показват, че необходимата степен на пречистване на водата от Mn е постигната само чрез комбиниране на озониране на вода с последващо третиране с коагулант, утаяване и филтриране чрез пясъчен филтър или двуслоен или въглероден филтър в случай на контактна коагулация.ефективността не зависи от дозата озон и коагулант (65). Озонирането се използва и в комбинация с UV лъчение (66).
Ефективно и технологично просто е използването на калиев перманганат като окислител (67), който окислява Mn (II) до слабо разтворим манганов оксид MnO (OH) 2. Фино диспергираната флокулентна утайка от манганов оксид MnO2, която има голяма специфична повърхност (около 300 m2 / g), ефективно сортира някои органични съединения и засилва процеса на коагулация, имащ заряд в диапазона на рН 5-11, който е противоположен на зарядите на продуктите на хидролизата на коагуланти - алуминиеви или железни хидроксиди (35).
С комбинираното присъствие на манган и желязо, включително колоидни форми на съединения на тези метали, при условия на ниски температури, ниска алкалност, ниска твърдост на водата, степента на неговото пречистване се увеличава чрез последователно третиране с KMnO 4 и H 2 O 2 ( 40). Методът на нанофилтрация с използване на Н2О2 се препоръчва като най -ефективният и най -евтиният метод (68).
Железните соли имат каталитичен ефект върху процеса на деманганиране, използвайки H2O2 (69). Известен е методът Fenton (70), където H 2 O 2 е окислител, Fe 2+ е катализатор и модифициран фентонов процес (66), който допълнително използва UV лъчение.
Практикува се да се извършва окислително унищожаване на замърсители на подземните води директно в кладенците, в които се инжектират окислителни реактиви, и да се транспортират продуктите на реакцията и излишните реактиви чрез потока на подземните води (71).
Биологичните методи се използват широко при пречистването на водата (35, 72, 73). Бактериите, консумиращи манган от този тип Бактерии манганикус, Metallogenium personatum, Caulococeus манганифер, Leptothrix lopholea, Leptothrix echinata (35, 75, 76) pedomicrobium manganicum(77), цианобактерии ( Цианобактерии) (78, 79). В резултат на усвояването на манган от водата се образува пореста маса, съдържаща голямо количество манганов оксид, който служи като катализатор за окисляването на Mn (II) (75). В зависимост от съдържанието на желязо, манган и наличието на други йони се използват различни видове филтри (35, 80), вкл. двустепенна (74), бавна (81) и т.н.
Като среда за обездвижване на бактерии, освен минерали, се използват синтетични влакна, които са неразтворими във вода, устойчиви на действието на микроорганизми и имат максимално развита повърхност за фиксиране на естествени биоценози (82). Като биоадсорбент се използва морското растение Vzmorin (Zostere L.) в оригиналната му или химически модифицирана форма, което има висока абсорбционна способност (83); биоценоза на съоръжения за биологично пречистване за производство на алкохол и млечни заводи (84).
Ефективността на методите за биологично отстраняване на желязо и манган е значително по -ниска от пречистването на реагентите на подземните води (73, 85).
Задоволителни резултати при отстраняването на манган се получават чрез коагулация с желязо или алуминиеви соли, въпреки че използването на алуминий неизбежно води до замърсяване на водата с остатъчен алуминий, който замества калция в човешките кости (29).
Железният хлорид в комбинация с водороден пероксид, последван от ултрафилтрация, ефективно отстранява желязото и мангана от води с повишено съдържание на органичен въглерод (86, 87). Предварителната обработка с окислители (хлорен диоксид и калиев перманганат) подобрява качеството на почистване и намалява дозата на коагуланта (88).
Използването на титанов коагулант (с по -висока скорост на флокулация) позволява да се намали обемът на утайката и дозата на въведения реагент, следователно, да се намали нивото на вторично замърсяване на остатъчния титан.
Алумосилициевият флокулант-коагулант, работи в диапазона на рН = 5,5-10 и премахва йони на преход и тежки метали, като ги свързва в неразтворими силикати (89). Електрокоагулацията премахва не само съединенията на желязото и мангана, но и силиция под формата на силициева киселина (90). Ефективността на пречистването от манган се увеличава с увеличаване на продължителността на процеса, което се обяснява с наличието на автокаталитична реакция с MnO2 и увеличаване на концентрацията на органични компоненти, подложени на предварителна коагулация (91).
Пречистването на водата с полифосфати се разглежда като метод за отстраняване на разтворимия манган и желязо от водата (92).
Ултрафилтрацията и нанофилтрацията се използват като последен етап на деманганиране в линиите за пречистване на вода (93-95). Мембраните позволяват да се задържат фино диспергирани и колоидни примеси, макромолекули, водорасли, едноклетъчни микроорганизми, кисти, бактерии и вируси, по -големи от 0,1 микрона. При правилно използване на апарата е възможно да се извърши избистряне и дезинфекция на вода без използване на химикали.
Mn с концентрация от 0,4 до 5,7 mg / L се отстранява почти напълно (96). На мембрани с кухи влакна с размер на порите 0,1 μm,> 93% Mn се отстранява при рН> 9,7 (97). За да се възстановят първоначалните характеристики на мембраните няколко пъти годишно, е необходимо химически промиване на мембранния апарат със специални киселинни и алкални реактиви за отстраняване на натрупаните замърсители. Освен това такива филтри не могат да се захранват с вода със сравнително високо съдържание на суспендирани твърди вещества. Анионните повърхностно активни вещества, когато се добавят към водата, образуват мицели, чийто размер е много по -голям от размера на порите на мембраната. Металните йони образуват комплекси с тези мицели и се задържат по време на филтрация с повече от 99%.
Използването на хелатни мембрани и мембрани от полисулфон, полиетерсулфон, поливинилиден флуорид, целулоза, регенерирана целулоза и др. Позволява, в допълнение към металните йони, ефективно да се отстранят и други замърсители (98, 99). Мембраните, изработени от синтетични (полиамиди, полиестери, ароматни полиамиди, полиакрилати), биологични (протеини, калоген) материали и активен въглен, са сходни по своето действие с мембраните за обратна осмоза (улавят големи аниони, Ca, Mg катиони, йони на тежки метали, големи органични съединения) и в същото време те имат висока пропускливост за малки йони на натрий, калий, хлор и флуор. Мембраните на основата на нановлакна са по -ефективни (100). За извличане на йони на тежки метали от повърхностни и подземни води е разработен принципно нов метод за образуване на филтриращ елемент, направен на базата на скални базалтови скали (101).
Препоръчително е да се използва йонообменният метод с едновременно дълбоко омекотяване на водата и освобождаването й от манган и желязо (102). Процесът се осъществява чрез филтриране чрез катионно зареждане с катионизация на натрий или водород по време на омекотяване на водата. Анионообменниците - органичните абсорбери дават възможност да се извлекат незначителни количества желязо, свързано с органични съединения, които не се отстраняват на филтри с каталитично зареждане (103).
В редица страни, включително Съединените щати (104, 105), методът за отстраняване на манган с помощта на манганов катионообменник стана широко разпространен. Катионообменникът на манган се приготвя от всеки катионообменник в натриева форма чрез последователно преминаване през него разтвор на манганов хлорид и калиев перманганат. Процесите, протичащи в този случай, могат да бъдат представени със следните реакции:
2Na [Cat] + MnCl 2 ->
Mn [Cat] 2 + 2NaCl
Mn [Cat] + Me + + KMnO 4 ->
2Me [Cat] + 2MnO 2,
където Аз +- катион Na +или K +.
Калиев перманганат окислява мангана, образувайки манганови оксиди, които се отлагат под формата на филм върху повърхността на зърната на катионообменника. Филмът се регенерира (възстановява) на катионообменник с разтвор на калиев перманганат. Консумацията на калиев перманганат за регенерацията на мангановия катионообменник е 0,6 g на 1 g отстранен манган (106). Съдържанието на манган по този метод се намалява до 0,1 mg / dm 3. Методът за отстраняване на манган с помощта на манганов катионообменник не е намерил приложение във вътрешната практика поради високата си цена.
Анализът на съвременното състояние на деманганиране на повърхностни и подземни води при приготвянето на питейна вода показва фундаменталното развитие и перспективите на методите за сорбция (107-109). Това са добре контролирани процеси, които ви позволяват да премахнете замърсителите с изключително широк характер (независимо от тяхната химическа устойчивост) до почти всяка остатъчна концентрация и не водят до вторично замърсяване.
Сорбентите трябва да имат развита или специфична повърхност с естествен или изкуствен произход (10). Процесът на сорбция се осъществява по метода на адхезионната обемна филтрация чрез зареждане в насипни вертикални филтри, като важно място се отделя на филтри с гранулирано зареждане (2).
Според съвременните теоретични концепции най -висок капацитет на задържане притежава товарът с максимална повърхност на контакт на частиците с вода и най -ниската хидродинамична сила на разделяне, както и най -високата междугранулна и отворена порьозност. В допълнение, той трябва да бъде силно устойчив на механично износване в кисели, алкални и неутрални среди (110-113).
Търговските микропорести адсорбенти обикновено имат пори с ефективни радиуси<1,5¸1,6 нм и с позиций современной технологии они могут быть названы ультрананопористыми. Именно такие адсорбенты обеспечивают высокую энергию и селективность адсорбции (114).
Исторически използването на сорбенти е свързано с микропорести въглеродни материали - активни въглени. Доскоро активният въглен (AC) беше най -добрият сорбент за пречистване и последващо пречистване на питейна вода, включително най -добрият - американски гранулиран активен кокосов въглен (ACC). Въглищата почистват водата от широк клас примеси - много органични примеси, остатъчен хлор, много форми на органичен въглерод и йони на тежки метали (115-118). Неговият сорбционен капацитет и ресурс обаче са малки. Това е скъп материал, нестабилен в агресивна среда, бактериите се размножават добре в него и изисква регенерация (107, 108, 119). За да се пречисти водата от катиони Mn 2+, повърхността на активен въглен се импрегнира с калиев перманганат (120, 121).
За пречистване на питейна вода се използват също сулфо въглища или неговата окислена форма (122), натрошен антрацит от марката Puralat (въглища с най -висока степен на коализация, съдържащи 95% въглерод) и неговите модификации, окислени по различни методи (116, 123).
Изследването на адсорбцията на Cu 2+, Ni 2+, Co 2+, Zn 2+ и Mn 2+ от водни разтвори върху въглища, получени от различни прекурсори и окислени по различни методи, и върху карбоксилна смола показа, че селективността на материали не зависи от метода и степента на окисляване, вида на прекурсора и адсорбента, структурата на порите (124).
Най -новото постижение на науката и технологиите са филтрите със силно реактивна въглеродна смес - HRCM (94, 125). Те добре пречистват водата от неразтворими примеси и микроорганизми, абсорбират нефтени продукти и разтворими в етер вещества до нива под MPC (скорост на пречистване повече от 1000), ефективно отстраняват много катиони (мед, желязо, ванадий, манган), органични и неорганични аниони ( сулфиди, флуориди, нитрати), намаляват концентрацията на суспендирани частици повече от 100 пъти. Наноструктурите, съдържащи се в HRCM, са графени (въглеродни атоми, подредени под формата на шестоъгълници), нанотръби, нанорини и нанофрактали. Частично счупените ковалентни връзки образуват огромен брой ненаситени междуатомни въглеродни връзки по периметъра на въглеродни шестоъгълни връзки в масата на HRCM. Ненаситените междуатомни въглеродни връзки (свободни радикали) в контакт с много широка група вещества (всички неразтворими и някои водоразтворими примеси) ги поддържат в насипно състояние, позволявайки на молекулите на водата да преминават през тях. HRCM задържа примеси както за сметка на свободните радикали на молекулярно и атомно ниво, без да влиза в химични реакции, така и чисто механично.
HRCM е представител на наноматериали, които включват нановлакна AlO (OH) и невлакнести фази на други оксиди и хидроксиди, ефективни сорбенти за отстраняване на Ni 2+, Fe 2+, Mn 2+, Zn 2+ и аниони As 3+, Като 5+, Cr 6+ (94). Въпреки това, въпреки че добре пречиства водата от неразтворени примеси, тя практически не премахва разтворимите.
Нов и обещаващ сорбционен материал, подходящ за пречистване на водата, макар и малко проучен, е естественият минерал шунгит (126-130). Шунгитите са предкамбрийски скали, наситени с въглеродна (шунгитова) материя в некристално състояние. Те се различават по състава на минералната основа (алумосиликатна, силициева, карбонатна) и количеството на шунгитовото вещество. На второ основание те се подразделят на нисковъглеродни (до 5% С), средновъглеродни (5-25% С) и високовъглеродни (25-80% С). Те са естествен композит с необичайна структура - равномерно разпределение на силно диспергирани кристални силикатни частици с размер около 1 микрона в аморфна въглеродна матрица.
Изгорял при температура 1100 ° C шунгит се използва като пълнители за филтърни касети на крайбрежни кладенци за засмукване на вода. Обещаващи на базата на шунгит са леки гранулирани и на бучки материали (при тяхното незначително водопоглъщане от 10-13%), получени чрез калциниране при 500-550 ° C за 2-3 часа, в резултат на което затворен клетъчен шунгизит се образуват гранули.
Шистите и продуктите от тяхната термична обработка имат сорбционни свойства по отношение на катиони на тежки метали и тежки нефтени фракции (131). Шисти са скали с паралелно (наслоено) подреждане на минерали. В състава доминира минералната част - калцит, доломит, хидрослюда, монтморилонит, каолинит, фелдшпати, кварц, пирит и др. Органичната част (кероген) е 10-30% от масата на скалата и само в най -високо качество шисти достига 50-70% ... Той е представен от био- и геохимично трансформирано вещество от най-простите водорасли, което задържа (таломоалгинит) или губи (колоалгинит) клетъчната структура. Променените остатъци от висшите растения (витринит, фузенит, липоидин) присъстват като примес.
Напоследък все по -често за пречистване на водата от съединения на тежки метали се използват невъглеродни сорбенти с естествен и изкуствен произход - минерални алумосиликати (различни глини, колби, цеолити, силициев диоксид и др.). Използването на такива сорбенти се дължи на тяхната селективност, доста висок сорбционен капацитет, свойства на катионообмен на някои от тях, относително ниска цена и наличност (като локален материал) (107, 108, 132-135). Характеризират се с развита структура с микропори с различни размери, в зависимост от вида на минерала. Те имат развита специфична повърхност, висока абсорбционна способност, устойчивост на влияния на околната среда, способност да ускоряват протичането на реакцията и могат да служат като отлични носители за фиксиране на различни съединения върху повърхността по време на тяхната модификация (136, 137).
Механизмът на сорбция на замърсителите върху тези материали е доста сложен, той включва ван дер Ваалсови взаимодействия на въглеводородни вериги с развита повърхност от силикатни микрокристали и кулоновско взаимодействие на заредени и поляризирани молекули сорбат с положително заредени участъци от повърхността на сорбента, съдържащ Н + и А1 3+ йони. При определени условия глинените материали ефективно адсорбират почти всички изследвани вируси: арбовируси, миксовируси, ентеровируси, растителни вируси, бактериофаги и актинофаги.
Така опоките (микропорести скали, съставени от аморфен силициев диоксид с примес от глинеста материя, скелетни части на организми, минерални зърна от кварц, фелдшпати и др.) Надвишават „черния пясък“ с повече от 1,5 пъти по сорбционен капацитет (138).
Активираният алумосиликатен адсорбент „Glint” се е доказал добре при пречистването на истински подземни води, съдържащи (mg / dm 3): Fe 2+ - 8,1; Mn 2+ - 7,9; H 2 S - 3,8 (135). Сорбционният капацитет на композитния сорбент от хумино -алуминиево -силициев диоксид достига 2,6 mmol / g за Fe 3+ и Mn 2+, 1,9 за Cr 3+ (139).
Глинените минерали монтморилонит, слюда (140), както и модифициран силициев диоксид (141) се използват в технологията за пречистване на водата.
Той сортира метални йони и багрила с различно естество, химически модифицирани с неутрален хитозанфероферицианиден комплекс вермикулит, минерал от групата на хидросиликатите със слоеста структура (142).
Естествените цеолити имат уникални адсорбционни, йонообменни и каталитични свойства. Зеолитите са водни калциеви алумосиликати с рамкова структура, съдържащи кухини, заети от йони и водни молекули, които имат значителна свобода на движение, което води до йонообмен и обратима дехидратация. Кухините и каналите в структурата на зеолитите могат да представляват до 50% от общия обем на минерала, което определя тяхната стойност като сорбенти. Формата и размерът на входните отвори на каналите, образувани от пръстени от кислородни атоми, определят стойностите на йони и молекули, които могат да проникнат в кухините на структурата на зеолита. Следователно второто им име е молекулярно сито.
Основните строителни единици на зеолитите са силициево-кислородни (SiO 4) и алуминиево-кислородни (AlO 4) тетраедри, свързани чрез кислородни мостове. В центровете на тетраедрите са силициеви и алуминиеви атоми. Алуминиевият атом носи един отрицателен заряд (той се намира в sp 3тетраедрична хибридизация), която обикновено се компенсира от положителния заряд на катиони на алкални или алкалоземни метали. Известни са повече от 30 вида естествени зеолити (143).
Естествените цеолити се използват под формата на прахове и филтриращи материали за пречистване на водата от повърхностноактивни вещества, ароматни и канцерогенни органични съединения, багрила, пестициди, колоидни и бактериални замърсители. Зеолитите са способни да изпълняват функциите на селективен филтър за извличане на цезий, арсений и стронций от вода (144). Степен на зеолит-клиноптилолит (Na 2 K 2 1OAI 2 O 3 10SiO 2) от находището Товуз (Азербайджан) беше успешно използван за пречистване на подпочвените води от желязо и манган, като преди това беше изложен на бариерен електрически разряд (145). Зеолитите могат да се използват с добавки от HRCM и диетиламиноетил целулоза в промишлени и битови филтри (146). Широко известен филтриращ материал Manganese Greensand (зелен пясък) на базата на зеолит (натриев глауконит), предварително обработен с разтвор на манганов хлорид, който служи като източник на кислород, окислява йони на двувалентен манган и желязо до тривалентни и утайки (103).
Високата механична якост на естествените цеолити дава възможност да се изключи операцията на гранулиране на адсорбент, което прави цената му няколко пъти по -ниска от цената на синтетичните цеолити. Сорбционният капацитет на зеолитите се увеличава с повишаване на температурата на водата (147).
Естествените и модифицирани минерали като бруцит, родохрозит, ксиломелан имат сорбционни и каталитични свойства по отношение на йони на манган и желязо (148).
Бруцитът е минерал, магнезиев хидроксид с понякога присъстващи изоморфни примеси на Fe (феробрузит) или Mn (манганобруцит). Кристалната структура на бруцита обикновено е наслоена. ОН йони образуват най -плътната шестоъгълна опаковка, в която всеки слой се състои от два плоски листа, успоредни на равнината (0001). Октаедричните кухини между хидроксилни йони са запълнени с йони Ме, като по този начин имат шесткратна координация (свързана с три йона ОН на един лист и с три йона на друг лист). Доказано е технологичното предимство на адсорбционните свойства на естествения бруцит Mg (OH) 2 пред зеолитите като активен сорбент за обещаващи технологии за пречистване на естествени и отпадни води (149). Термичната модификация на естествен минерал при 400-600 ° C причинява структурни промени на повърхността, които настъпват по време на дехидратацията на сорбента, които увеличават сорбционната активност на бруцита по отношение на мангановите йони в присъствието на желязо от желязо (150). Ултразвуковото лечение засилва кинетиката на сорбцията на метали върху бруцит. Десорбцията на метали и регенерирането на сорбента се извършват ефективно чрез третиране с разтвори на солна киселина и амоняк (151).
Филтрирането през гранулирана среда с каталитични свойства понастоящем се счита за най -обещаващия метод за пречистване на водата от манган. Съдържащите се в изходната вода йони на двувалентен манган се окисляват от разтворения кислород във въздуха в присъствието на катализатор, превръщат се в неразтворими манганови съединения и се разделят от натоварващия слой.
По-високи манганови оксиди, отложени по един или друг начин върху гранулирана матрица от филтри (152-158), служат като катализатори. На матрица с естествен произход (кварцов пясък, доломит, експандирана глина, алумосиликат, естествени и изкуствени цеолити или други материали) се нанася филм от манганови или железни оксиди или тези оксиди се въвеждат в структурата. На зърната на такива товари се случва окисляване с едновременното задържане на окислени вещества.
Кислородът, съдържащ се във водата, е достатъчен за окисляване на малки количества желязо, когато водата преминава през каталитичен слой като Birm, Greensand и др. Полученият хидроксид остава върху зареждащото легло. При липса на кислород във водата се получава окисление на желязо поради редукцията на желязото и мангановите оксиди от повърхността на частиците.
Манганът се отстранява при високи концентрации и независимо от формата, в която се намира, както от кладенеца, така и от чешмяната вода. В същото време суспендираните частици и естествената органична материя се отстраняват от водата (159). Ефективността на катализатора намалява в резултат на измиването от частиците оксиди. Ако желязото присъства във водата заедно с манган, тогава нивото на рН не трябва да надвишава 8,5. Някои зърнени товари не се нуждаят от възстановяване, докато други го правят. По този начин Birm е малко подложен на физическо износване и остава ефективен в широк диапазон от температури на захранващата вода (29). Окислените вещества се отстраняват чрез обратно промиване.
Каталитичните свойства на процеса на окисляване на разтворимия манган до манганов оксид се притежават от заряд от манганова руда от карбонатен тип, термично модифициран при 400-6000 ° С в продължение на поне 30 минути. Зареждането не изисква химическа регенерация, което опростява и намалява разходите за процеса (160).
Манганови руди от оксидни типове и неорганични йонообменници на базата на термично модифицирани оксиди на манган (III, IV) също имат каталитични свойства (161-163). Известен филтриращ материал, съдържащ два компонента: естествен минерал (руда) с най -малко 80% манганов диоксид и варовик, в повърхността на който е импрегниран манганов оксид (164).
Зареждането от натрошен пиролузит и въвеждането на въздух под налягане правят възможно съвместното отстраняване на Mn 2+ и NH 4 + (165). Процесът е ефективен поради проникването на кислород във всички зони по профила на филтърния реактор. Неорганичните сорбенти на основата на смеси от манганови (III, IV) и титанови (III, IV) оксиди имат повишени сорбционни характеристики (обменна способност) и подобрени експлоатационни свойства (слепване, механична якост) (166).
Псиломеланът е катализатор за окисляването на манган и / или желязо до слабо разтворими оксиди (167). Той осигурява гарантирано качество на пречистване на водата в рамките на максимално допустимата концентрация, опростява и намалява разходите на процеса, като елиминира операцията на варуване и по -икономичен режим на измиване на филтърната среда.
Вътрешните каталитични пълнежни материали MZhF и DAMF са направени на базата на естествен доломитов материал, съдържащ калциеви и магнезиеви карбонати. Те са твърда буферна система, която регулира рН на водата и поддържа леко алкална реакция в нея, която е оптимална за процеса на размразяване.
Доломитът обикновено е двоен карбонатен минерал с идеалната формула CaMg (CO 3) 2. Смята се, че се образува чрез заместване на калциев карбонат (калцит), в резултат на което се образуват и задържат пори, тъй като CaCO 3 има по -малък моларен обем (168). Перспективата за използване на доломит като филтрираща среда е описана в (168-171). Доломитът, загрят при 700-800 ° C в кипящ слой, усилва извличането на метали от вода (172-174). Сорбентът на основата на доломит, изгорен на въздух при 500-900 0 C за 1-3 часа и обработен с разтвор, съдържащ двувалентни манганови йони (Mn 2+ ~ 0,01-0,2 mol / dm 3), има висока сорбционна способност и ефективно пречиства вода от манган и желязо до стойности, много по -ниски от допустимите санитарни стандарти (175).
Като сорбент може да се използва карбонатната скала от Болшеберезинското находище, обработена с магнезиеви соли за увеличаване на сорбционния капацитет (176).
Както показват проучванията, проведени понастоящем в Института по колоидна химия и химия на водата на Националната академия на науките на Украйна (177), много обещаващ катализатор на сорбент, получен от оксидно-карбонатна манганова руда от находището Никопол (Днепропетровска област , Украйна) чрез термичната му обработка при температура 450 -800 0 С, последвана от модификация с разтвор на калиев перманганат с концентрация 0,2-0,5 тегл.%. Мащабни изпитания на синтезирания сорбент в процеса на деманганиране на подземните води на експлоатационните кладенци на водохващането Чернишевски в град Мукачево (Mn 1,77-1,83 mg / dm 3) и в селото. Русанове, Киевска област (Mn 0,82-0,88 mg / dm 3) показа високата си сорбционна способност и възможността за пълно извличане на манган от вода.
Има доклади за перспективите за използване на силно диспергирани сорбенти с магнитни свойства (178 179). При метода на нереагентна магнитна сорбция водата се смесва с фино диспергиран парамагнитен материал, който образува комплекси с метални йони. Последващата обработка с високо градиентно магнитно поле или филтриране през слой от тънка стоманена тел с известно ниво на намагнитване премахва образуваните комплекси. Метод на PH-смяна: рН на пречистената вода преди етапите на пречистване се променя локално, докато замърсяването се отлага на различни етапи на пречистване при сорбция, които се регенерират чрез обратната промяна на рН на средата.
С всички многобройни доклади за различни методи за деманганиране на естествени води, те се основават на окисляването на двувалентни манганови йони до четиривалентно състояние и отделянето на продуктите на реакцията от течната фаза, главно върху филтърни среди в резултат на адсорбция, хемосорбция или каталитично окисляване. Както показват проучванията от последните години, най -обещаващият филтриращ материал за отстраняване на манганови съединения от пречистената вода са естествени минерали, термично или химически модифицирани с неорганични съединения. Като се има предвид нарастващото търсене в Украйна за използване на подземни води, привличането за тези цели на евтини битови суровини (например оксидно-карбонатна руда от Никополското находище, закарпатски клиноптилолит и др.) Представлява интерес както поради тяхното ефективност и от икономическа гледна точка.
ЛИТЕРАТУРА:
- Suyarko V.G., Krasnopolsky N.A., Shevchenko O.A. За техногенните промени в химичния състав на подземните води в Донбас // Известия вузов. Геология и проучване. - 1995. - No1. - стр. 85 - 90.
- Хуаларян М. Г. Антропологическо въздействие върху природата на Севера и неговите екологични последици // Материали от общоруската среща и заминаване. научни. сес. Разделения океанол., Nat. атмосфера. и геогр. РАН „Проблеми с водата в началото на века”, 1998 г., Институт на Пробл. бал. с шипове. Север.- Апатит: Издателство Колск. научни. център на РАН. - 1999.- С. 35- 41.
- Екологична оценка на настоящото състояние на повърхностните води на Украйна (методически аспекти). Динисова О.И., Серебрякова Т.М., Чернявска А.П. та в // Укр. географ. журн. - 1996. - No 3. - С. 3 -11.
- Изследване на антропогенния товар върху трансграничните реки на Беларус и Украйна, стабилизиране на тяхното състояние. Yatsyk A.V., Voloshkina V.S., Byshovets L.B. et al. // EKVATEK-2000: 4th International. Congr. „Вода: екологична. и технол. Москва, 30 май - 2 юни 2000 г. - М.: SIBIKO Int. - 2000.- S.208- 209.
- Risler J.J., Charter J. Управление на подземните води във Франция. // Инст. Вода и околна среда. Управление. - 1995. - 9, №3. - Р. 264 - 271.
- Каменский Г. Ю. Актуални проблеми на експлоатацията на подземните води в Московска област // Санитарно инженерство.- 2006.- № 4.- С. 68-74.
- Алферова Л. И., Дзюбо В. В. Подземни води на Западносибирския регион и проблеми с използването им за водоснабдяване с питейна вода // Води. домакинства в Русия.- 2006.- No 1.- С. 78-92
- Кулаков В. В. Екологични проблеми на използването на сладките подземни води за питейно водоснабдяване на населението на Хабаровска територия // Матер. conf. в подготовка за Всеруския. конгрес по опазване на природата, Хабаровск, 15 март 1995 г. - Хабаровск .. - 1995. - с. 49 - 50.
- Глушкова К.П., Балакирева С.В. Получаване на питейна вода на находищата на Нижневартовското предприятие за производство на нефт и газ ОАО ННП // Научно -техническа конференция на студенти, аспиранти и млади учени от Уфийския държавен петролен технически университет, Уфа, 2005. Сборник с резюмета . Книга. 2.- Уфа: USPTU 2005.- S. 209-210.
- А. К. Заполски Водоснабдяване, водоснабдяване и качество на водата. - Киев: училище „Вища”, 2005. - 671с.
- Романенко В.Д. Основи на хидроекологията.- Киев: Генза, 2004.- 662 с.
- Повърхностни и подземни води. Морски води. От държавния доклад „За състоянието и опазването на околната среда на Руската федерация през 2003 г.“. // Екологичен бюлетин на Русия. - 2005. - No 3. - стр. 53 - 60.
- Лукашевич О.Д., Патрушев Е.И. Пречистване на водата от съединения на желязо и манган: проблеми и перспективи // Известия вузов. Химия и химия. технология. - 2004. - 47, No1. - С. 66 - 70.
- Чън Хонг-ин, Чън Хонг-пинг. Проблеми на еутрофикацията при производството на питейна вода // Zhejiang gongue daxue xuebao = J. Zhejiang Univ Technol. - 2002. - 30, бр.2. - Р. 178 - 180.
- Джонсън Карън Л., По -младият Пол Л. Дж. Бързо отстраняване на манган от минни води с помощта на биореактор L.J. // Околна среда. Качествено. - 2005. - 34, бр.3. - Р. 987 - 993.
- Labroue L., Ricard J. Du manganese dans l'eau pampee: de l'importance de bieu implanfer les captages. // Adour-Garonne. - 1995. - No 62. - С. 17 - 20.
- Лукашевич О.Д. Проблеми на пречистването на водата във връзка с промяна в състава на подземните води по време на експлоатацията на водоприемниците (По примера на юг от Томска област) // Химия и технология на водата.- 2006.28, No 2.- С. 196-206.
- SNiP 2.04.02-84. Водоснабдяване. Външни мрежи и структури // Госстрой СССР - М.: Стройиздат, 1985. - 136 с. (заменете с украински SNiP) DSanPin „Питейна вода. Гигиенични вимоги към качеството на водата и централизираното държавно водоснабдяване ". - Одобрен от Министерството на здравеопазването на Украйна, Заповед № 383 от 23 декември 1996 г.
- Насоки за осигуряване на качеството на питейната вода. III изд., Т1 (препоръки) // Световна здравна организация. - Женева, 2004 г. - 58 стр.
- Жаба Б.Н. Пречистване на водата. - М.: Издателство на Московския държавен университет, 1996. - 680 с.
- Човек. Медицински и биологични данни // Публ. № 23 на Международната комисия по радиологична защита. - М.: Медицина, 1997.- С. 400-401.
- Авцин А.П., Жаворонков А.А., Риш М.А., Строчкова Л.С. Човешка микроелементоза. - М.: Медицина, 1991 - 496 с.
- Tasker L, Mergler D, Hellier G, Sahuquillo J, Huel G. Манган, нивата на моноаминовия метаболит при раждането и детското психомоторно развитие // Невротоксикология- 2003.-- P.667-674.
- Lutskiy Ya.M., Ageikin V.A., Belozerov Yu.M., Ignatov A.N., Izotov B.N., Neudakhin E.V., Chernov V.M. Токсични ефекти върху децата на химикали, съдържащи се в опасни концентрации в околната среда // Мед. аспекти на ефекта от ниските дози радиация върху тялото на деца, юноши и бременни жени. - 1994. - No2. - С. 387 - 393.
- Илченко С.И. Клинични, имунохимични и цитогенетични диагностични критерии за преносологични нарушения на здравето на деца от мангановата рудна област на Украйна. Резюме на дипломната работа. Канд. дис. - Киев, 1999. - 19 с.
- Горбан Л.Н., Лубянова И.П. Съдържанието на манган в косата като тест за излагане на стоманени заварчици // Актуални хигиенни проблеми. регламенти. хим. фактори в обектите на околната среда. Резюмета. доклад Vses. conf. 24-25 окт. 1989.- Перм. - 1989. - С.51 -52.
- Мелникова М.М. Манганова интоксикация // Трудова медицина и индустриална екология. - 1995.- No6. - С.21-24.
- Sistrnk C., Ross M.K., Filipov N.M. Директен ефект на манганови съединения върху допамина и неговия метаболит Dopac: An in vitro стадия // Екологична тейкология и фармакология.-- 23.- С. 286-296.
- Рябчиков Б.Е .. Съвременни методи за обезвъздушаване и деманганиране на естествена вода // Енергоспестяване и пречистване на водата. - - No 6.- С.5-10.
- Guidoff T I., Audette R.J., Martin C.J. Тълкуване на профила за анализ на следи от метали за пациенти, изложени на работното място на метали // Ocupp. Med. -1997 -30. R 59-64.
- Nachtman J.P., Tubben R. E., Commissaris R.L. Поведенчески ефекти от хроничното приложение на манган при плъхове: изследвания на двигателната активност // Невро -поведенческа токсичност и тератология. - - № 8. - С. 711-717.
- Золотова Е.Ф., Ass HYu. Пречистване на вода от желязо, манган, флуор и сероводород. - М: Стройиздат, 1975.- 89 с.
- Николадзе Г.И. Подобряване качеството на подземните води. - М.: Стройиздат, 1987.- 240 с.
- Николадзе Г.И. Минц Д.М., Касталски А.А. Подготовка на вода за битово и питейно и промишлено водоснабдяване. - М.: Мир, 1989.- 97 с.
- Гончарук В.В., Якимова Т.И. Използването на нестандартни подземни води при водоснабдяване с питейна вода // Химия и технология на водата. - 1996. - 18, No 5, стр. 495-529.
- Руденко Г.Г., Гороновски И.Т. Отстраняване на примеси от естествени води при водопроводи. - Киев: Будивелник, 1976. - 208 с.
- Манган и неговите съединения. Кратък международен документ за оценка на химичните вещества 12. Световна здравна организация, Женева, 1999 г.- 69 с.
- Скот Дюрел Т, Макнайт Даян М., Валкер Бетина М., Хрнсир Дуейн С. Редокс процеси, контролиращи съдбата и транспорта на манган в планински поток // Околна среда. и Технол. - 2002. - 36, бр.3. - P453-495.
- Ким А.Н., Бекренев А.В. Отстраняване на желязо и манган от водата // Водоснабдяване на Санкт Петербург Държавно унитарно предприятие „Водоканал SP” SPb: Нов. е. - 2003.- С. 646- 676.
- Потупване. 2238912 Русия, MPK7 C 02 F 1/64, 1/58/Link Yu.A., Gordin K.A., Selyukov A.V., Kuranov N.P. // Метод за пречистване на питейна вода. - Публ. 27 октомври 2004 г.
- Драхлин Е.Е. // Научен тр. АКХ „Водоснабдяване“ - М.: ОНТИ АКХ, 1969. - Бр. 52, № 5. - 135 стр.
- Отстраняване на желязо, манган и сероводород. Сайтът на компанията LLC "HydroEcology". http: // www. hydroeco.zp.ua/
- Olsen P, Henke L. Предварителна обработка за филтриране с окисляване и задържане // Water Cond. И Пуриф. - 1995. - 36, бр.5. - R 40, 42, 44 - 45.
- Пестриков С.В., Исаева О.Ю., Сапожникова Е.И., Легуш Е.Ф., Красногорская Н.Н. Теоретично обосноване на технологията на окислително деманганиране на вода // Ing. екология. - 2004. - No 4. -С. 38-45, 62-63.
- Йодтовски Анджей. Badania nad przebiegiem koagulacj? zanieczyszcze? w? d powierzchniowych poprzedzonej utlenianiem // Zesz. наук Пъпка. Plodz.1994 г. - No 43. - С. 167 - 190.
- Гришин Б. М., Андреев С. Ю., Саранцев В. А., Николаева С. Н. Дълбоко последващо пречистване на отпадъчните води чрез каталитична филтрация // Международна научно-практическа конференция „Проблеми на инженера. осигуряване и екология на градовете ”, Пенза, 1999. Сб. мат -ин. - Пенза: Издателство Приволж. къщи на знанието. - 1999.- С. 102- 104.
- Потупване. 2181342 Русия, MPK7 C 02 F 1/64, C 02 F 103/04/Lukerchenko V.N., Nikoladze G.I., Maslov D.N., Khrychev GA., Titzhani Shabi Mama Akhmed // Метод за комбинирано извличане на желязо и манган от вода. - Публ. 04.2002 г.
- Winkelnkemper Heinz. Unterirdische Enteisenung и Entmanganung // WWWT: Wasserwirt. Wasser-techn. - 2004. - No 10. - S.38 - 41.
- В. В. Кулаков Хидрогеологични основи на технологията за обезвъздушаване и деманганиране на подземните води в водоносния хоризонт // Материали на Всеруската среща по подземните води в Сибир и Далечния изток. (Красноярск, октомври 2003 г.). - Иркутск; Красноярск: Издателство ИСТУ - 2003. - С.71-73.
- Заявка 10033422 Германия, IPC7 C 02 F 1/100, E 03 B 3/06/H? Gg Peter, Edel Hans-Georg // Verfahren und Vorrichtung f? R die Behandlung eisen und manganhaligen Grundwassers mit Grundwasserzirzirkulationsbrunnen. - Публ. 17 януари 2002 г.
- Приложение UK 2282371 MKI6 C 02 F 1/24. 1/64 / Fenton B. // Отстраняване на манган от водоизточници в система за флотация на разтворен въздух. -Публ. 04/05/95.
- Уилмарт У.А. Отстраняване на желязо, манган и сулфиди. / Водни отпадъци Инж. 1988.-5, No 54.-P134-141.
- Zudemann D., Hasselbarth U. Die biologische Enteisenung und Entmanganung. - Фон Васер, 1971, Bd. 38.
- Луис Пинто А., Сесилия Ривера. Намаляване на желязото и мангана в порестите води на залива Консепсион и прилежащия континентален шелф по време на събитието „1997-98 EL NIO“ Cyil. Soc., 48, номер 3, 2003 г.
- Бахир В.М. Дезинфекция на питейна вода: проблеми и решения // Вода и екология.- 2003.- No 1.- С. 13-20.
- Йодтовски Анджей. Badania nad przebiegiem koa- gulacj? zanieczyszcze? w? d powierzchniowych poprzedzonej utlenianiem // Zesz. наук Plodz. 1994. - No 43. - С. 167-190.
- Савиняк Валдемар, Ктос Марчин. Zastosowanie Filtr? W Dyna Sand do od? Elaziania I odmangania- nia w? D podziemnych do? Wiadczenia eksploatacyjne // Ochr. ? път. - 2005. - No 3. - S.55-56.
- Ягуд Б. Ю. Хлорът като дезинфектант - безопасност при употреба и проблеми със замяната с алтернативни продукти // 5 -ти международен конгрес ECWATEK -2002. Вода: екология и технологии. 4-7 юни 2002 г. С. 68-72.
- Д -р Кожевников А.Б .; Петросян О.П., д.м.н. За тези, които не обичат хлор // StroyPROFIL - 4, №1. С. 30-34.
- Lytle C.M., C.M., McKinnon C.Z., Smith B.N. Натрупване на манган в крайпътна почва и растения // Naturwissenschaften. - 1994. - 81, No 11. - R 509-510.
- Можаев Л. В., Помозов И. М., Романов В. К. Озониране при пречистване на вода. История и практика на приложение // Пречистване на водата. - 2005. - No 11. - С. 33-39.
- Липунов И.Н., Санакоев В.Н. Подготовка на питейна вода за водоснабдяване. Социална икономика и екологични проблеми на горския комплекс. Резюмета. доклад международни k-техническа конференция. Екатеринбург. - 1999.- С. 231- 232.
- Ху Джи-гуан, Чанг Дзин, Чанг Ай-линг, Хуй Юан-фън. Приготвяне на питейна вода в процесите на озониране и третиране на биофилтър // Huabei dianli daxue xuebao = J. N. China Elec. Power Univ- 2006.- 33, No 1.- R 98-102.
- Разумовски Л.М. Кислород - елементарни форми и свойства. - М.: Химия, 1979. - 187 с.
- Гончарук В. В., Вакуленко В. Ф., Горчев В. Ф., Захалявко Г. А., Карахим С. А., Сова А. Н., Муравьев В. Р. Пречистване на днепровската вода от манган // Химия и технология. вода. - 1998. - 20, бр.6. - С. 641-648.
- Мунтер Рейн, Прейс Сергей, Калас Юха, Трапидо Марина, Вересенина Елена. Разширени окислителни процеси (AOPs): Технология за пречистване на водата за двадесет и първи век // Kemia-Kemi. - 2001. - 28, №5.Р 354-362 ..
- Уанг Гуй-ронг, Джан Цзе, Хуан Ли, Чжоу Пи-гуан, Танг Ю-яо. Zhongguo jishui paishui. Използването на три вида окислители при приготвянето на питейна вода // Китайска вода и отпадни води. - 2005. - 21, №4. - P37 -39.
- Potgieter, J. H., Potgieter-Vermaak, S. S., Modise, J., Basson, N. Отстраняване на желязо и манган от вода с високо зареждане на органичен въглерод. Част II: Ефектът от различни адсорбенти и нанофилтрационни мембрани // Биомедицински науки и науки за живота и Науки за Земята и околната среда.- 2005.- 162, № 1-4- С.61-70.
- Патент на САЩ 6,558,556. Khoe, et al. // Желязо-катализирано окисляване на манган и други неорганични видове във водни разтвори. - 6 май 2003 г.
- Лю Уей, Лян Йонг-Мей, Ма Джун. Отстраняване на манган от вода, като се използват железни соли като окислител на предварителен етап // Harbin gongue daxue xuebao = J. Harbin Inst. Технол. - 2004. - 37, бр.2. - R.180 - 182.
- Touze Solene, Fabre Frederique. L'oxydation in situ Experiences et criteres d'application // Eau, ind., Неприятности. - 2006.- No 290.- R 45-48.
- Назаров В.Д., Шаяхметова С.Г., Мухнуров Ф. Х., Шаяхметов Р.З. Биологичен метод на окисляване на манган във водоснабдителната система на град Нефтекамск // Вода и екология: проблеми и решения.- - No 4.- С.28 - 39.
- Ли Донг, Ян Хонг, Чън Ли-ксуе, Джао Ин-ли, Джан Дзи. Отстраняване на желязо и манганови йони от водата по време на приготвянето й // Beijing gongue daxue xuebao = J. Beijing Univ Technol. - 2003. - 29, №3. - R328-333.
- Ли Донг, Ян Хонг, Чън Ли-ксуе, Джан Цзе. Изследване на механизма за отстраняване на Fe 2+ с помощта на въздушна и биологична технология за отстраняване на Fe 2+ и Mn 2+ // Beijing gongue daxue xuebao = J. Beijing Univ. - 2003. -29, No 4.- R 441-446.
- Ли Донг, Джан Дзи, Уанг Хонг-тао, Ченг Донг-бей. Quik stsrt-up на филтър за биологично отстраняване на желязо и манган // Zhongguo jishui paishui. Китай Водни и отпадни води-2005. -21, № 12.-P 35-38.
- Потупване. 2334029 Великобритания, IPC6 C 02 F 3/10 / Hopwood A., Todd J. J.; Джон Джеймс Тод -Публ. Среда за пречистване на отпадъчни води 11.08.99.
- Патент на САЩ 5 443 729 22 август 1995 г. Sly, et al. Метод за отстраняване на манган от вода. Метод за отстраняване на манган от вода.
- Pawlik-Skowronska Barbara, Skowronski Tadeusz. Si-nice I ich interakcjd z metalami ciezkimi // Wiad.bot. - 1996. - 40, No 3 - 4. - С. 17-30.
- Потупване. 662768 Австралия, MKI5 C 02 F 001/64, 003/08. Хитър Линдзи, Арунпайроджана Вулапа, Диксън Дейвид. Метод и апарат за отстраняване на манган от вода. Университетът в Гуенсланд; общностна и промишлена изследователска организация. - Публ. 14.09.95.
- Ма Фанг, Ян Хай-ян, Уанг Хонг-ю, Джан Ю-хонг. Пречистване на вода, съдържаща желязо и манган // Zhongguo jishui paishui = Китайска вода и отпадни води. - 2004. - 20, бр.7. - P6-10.
- В. В. Комков Кондициониране на естествени води с високо съдържание на желязо и манган. Градско планиране: Резюмета. доклади за резултатите от научно -техническите. conf. VolgGASA. - Волгоград. - 1996.- С. 46-47.
- Журба М.Г., Орлов М.В., Бобров В.В. Обезвъздушаване на подземните води с помощта на биореактор и хидроавтоматичен филтър с плаващ товар // Проблеми на екологията по пътя към устойчивото развитие на регионите: (Международна научно-практическа конференция, Вологда, 17-19 май 2001 г.). Вологда: Издателство на ВОСТУ. - 2001.- С. 96-98.
- Заявка 10336990 Германия, IPC 7B 01 J 20/22, B 01 D 15/08. Bioadsorbens zur Entfernung von Schwermetallen? Us w? Ssrigen L? Sungen Inst. F? R nichtklassische Chemie e. V an der Univ. Лайпциг Хофман J? Rg, Wecks Mike, Freier Ute, Pasch Nicoll, Gemende Bernhard. - Публ. 10.03.2005 г.
- Никифорова Л.О., Павлова И.В., Белополски Л.М. Влияние на съединенията на желязото и мангана върху биоценозата на съоръженията за биологично пречистване // Химична технология. - 2004. - No1. - стр. 31-35.
- Чън Ю-хуей, Ю Дзян, Се Шуй-бо. Отстраняване на желязо и манган от подземните води // Gongue yongshuiyu Feishui = Ind. Вода и отпадни води. - 2003. - 34, бр.3. - P1-4.
- Potgieter J.H., McChndle R.I., Sihlali Z., Schwarzer R., Basson N. Отстраняване на желязо и манган от вода с високо зареждане на органичен въглерод Pt I Ефектът на различни коагуланти // Вода, въздух и замърсяване на почвата. - 2005. - 162, No 1-4. - R 49 - 59.
- Potgieter J.H., Potgieter Vermaak S.S., Modise J., Basson N. Отстраняване на желязо и манган от вода с високо зареждане на органичен въглерод Част II. Ефектът на различни адсорбенти и мембрани за нанофилтрация // Вода, въздух и замърсяване на почвата. - 2005. - 162, No 14. - R.61-70.
- Йодтовски Анджей. Badania nad przebiegiem koa- gulacj? zanieczyszcze? w? d powierzchniowych poprzedzonej utlenianiem // Zesz. наук Plodz.1994 г. - No 43. - R 167-190.
- Алексиков А.Е., Лебедев Д.Н. Използването на неорганични коагуланти в процесите на пречистване на водата // Материали на Международния научен симпозиум „Безопасност на живота, 21 век“, Волгоград, 9-12 октомври 2001 г. -Волгоград: Издателство „ВолГАСА“. - 2001, стр. 140 -141.
- Белов Д. П., Алексеев А. Ф. Съвременни технологии за приготвяне на питейна вода и пречистване на изплакващите води на станциите за обезгладяване „Водопад“ // 14 -та научно -практическа конференция на млади учени и специалисти „Проблеми на развитието на газовата промишленост на Западен Сибир“, Тюмен, 25 -28 април, 2006: .- Сборник с резюмета. Тюмен: Издателство на LLC "ТюменНIIгипрогаз" .. 2006.- С. 242-244.
- Bian Ruing, Watanabe Yoshimasa, Ozawa Genro, Tambo Norinito. Пречистване на водата от естествени органични съединения, желязо и манган чрез комбинирания метод на ултрафилтрация и коагулация // Suido Kyokai zasshi = J. Jap. Водни работи доц. - 1997. - 66, бр.4. - P24 -33.
- Mettler, S .; Абделмула, М .; Hoehn, E .; Schoenenberger, R .; Weidler, P; Гюнтен, У. фон. Характеризиране на утайки от желязо и манган от инсталация за пречистване на подземни води in situ // Национална асоциация на подземните води. - 2001.- 39, No6. - R.921 - 930.
- Chabak A.F. Филтриращи материали // Пречистване на водата. - 2005, No 12.- С. 78-80.
- Савелиев Г.Г., Юрмазова Т.А., Сизов С.В., Даниленко Н.Б., Галанов А.И. Наноматериали при пречистване на вода // Int. „Нови обещаващи материали и технологии за тяхното производство (NPM) - 2004”, Волгоград, 20 - 23 септември 2004 г .; Сб. научни. работи Т1. Раздел Наноматериали и технологии. Прахова металургия: Политехническа; Волгоград: Издателство ВолгГТУ - 2004. - с. 128 -150.
- Патент на САЩ 5 938 934, 17 август 1999 г. Balogh, et al. Наноскопични гъби на основата на дендример и метални композити.
- Suzuki T, Watanabe Y, Ozawa G., Ikeda K. Отстраняване на манган при пречистване на вода по метода на микрофилтрация // Suido kyokai zasshi = J. Япония Водни работи доц. - 1999. - 68, бр.2. - R 2-11.
- Хуан Цзян-юан, Ивагами Йошиюки, Фуджита Кенджи. Отстраняване на манган чрез микрофилтрация с контрол на рН // Suido kyokai zasshi = J. Jap Water Works доц. 1999. - 68. - No 12. - С. 22 - 28. Яп.: Рез. Английски
- Фанг Яо-яо, Дзен Гуан-мин, Хуан Дзин-хуей, Сю Ке. Отстраняване на метални йони от водни разтвори, като се използва процес на ултрафилтрация, подобрен с мицели // Huanjing kexue = Environ. - 2006.- 27, No 4.- R 641-646.
- Санг-Чул Хан, Кван-Хо Чоо, Санг-Джун Чой, Марк М. Бенджамин. Моделиране на отстраняване на манган в хелатни полимерно-асистирани мембранни системи за пречистване на водата // Journal of Membrane Science.- No. 290.- P 55-61.
- М. Иванов М. М. Тенденции в развитието на филтриращи материали // Вестник Aqua-term.- 2003.- №6 (16).- стр. 48-51.
- Лебедев И.А., Комарова Л.Ф., Кондратюк Е.В. Ползунов. Пречистване на желязосъдържащи води чрез филтриране през влакнести материали // Вестн. - 2004. - No 4. - стр. 171-176.
- Монетни дворове D.M. Теоретични основи на технологията за пречистване на водата. -М.: Стройиздат, 1964.- 156 с.
- Рябчиков Б.Е .. Съвременни методи за обезвъздушаване и деманганиране на естествена вода // Енергоспестяване и пречистване на водата. - - No 1. - С. 5-9.
- Конър Д.О. Премахване на желязо и манган // Водни канализационни работи. 1989. № 28. P68-78.
- Рейн Мунтер, Хелди Оясте, Йоханес Сът. Завършено отстраняване на желязо от подземни води // J Envir. Engrg.-2005.- 131, No 7.- P 1014-1020.
- Уилмарт У.А. Отстраняване на желязо, манган и сулфиди // Водни отпадъци Инж. - 1988.- 5, No 54.- С.134-141.
- Когановски А. М., Адсорбция и йонен обмен в процесите на пречистване на водата и пречистване на отпадни води, Киев: Наук Думка, 1983, 240 стр.
- Смирнов А. Д. Пречистване на сорбционна вода.- Ленинград: Химия., 1982.- 168 с.
- Чернова Р. К., Козлова Л. М., Мизникова И. В., Ахлестина Е. Ф. Естествени сорбенти. Аналитични възможности и технологично приложение // Актуални проблеми на електрохимичната технология: сборник от статии на млади учени. -Саратов: Издателство на SSTU-2000.-С. 260-264.
- Melzer V. 3., Apeltsina E. I. Използване на различни филтриращи материали за зареждане на филтри // Соврем, Технол. и оборудват. за обработка. вода за пречистване на водата. Изкуство. / Департамент по жилища-комуни, x-va Gos-система на Русия, Изследователски институт на общините. водоснабдяване. и пречистване на водата. - М., 1997 - С. 62-63.
- Плетнев Р. Н. Химия и технология за пречистване на водата в района на Урал: Инф. матер. RAS. - Екатеринбург. - 1995.- 179 с.
- Назаров В.Д., Кузнецов Л. К. Изследване на активни филтриращи материали за обезвъздушаване на подземните води // Сб. tr. архитекти-строежи, фак. Уфим. състояние масло. технология университет / Уфим. състояние масло. технология un-t. - Уфа, 1997 - С. 106-109.
- Шибнев А.В. Предварителна оценка на свойствата на някои филтриращи материали // Пестене на енергия и пречистване на водата. - 2001. - No1. - С. 87 -88.
- Ходосова Н.А., Белчинская Л.И., Стрелникова О.Ю. Въздействие на импулсно магнитно поле върху термично обработени нанопорести сорбенти. // Химия, физика и технология на повърхността на наноматериали IXP IM. ОО Чуйка Национална академия на науките на Украйна, Киев, 28-30 май 2008 г., стр. 263.
- Kumar Meena Ajay, Mishra G.K., Rai PK., Rajagopal Chitra, Nagar PN. Отстраняване на йони на тежки метали от водни разтвори с използване на въглероден аерогел като адсорбент // J. Hazardous Mater. - 2005. - 122, No 1-2. - Р162 -170.
- Шибнев А.В. Предварителна оценка на свойствата на някои филтриращи материали // Пестене на енергия и пречистване на водата. - 2001. - No1. - С. 87
- Протопопов В.А., Толстопятова Г.В., Мактаз Е.Д. Хигиенна оценка на нови сорбенти на базата на антрацити за пречистване на питейна вода // Химия и технология на водата. - 1995. - 17, No 5. - С. 495-500.
- Цинберг М.Б., Маслова О.Г., Шамсутдинова М.В. Сравнение на филтриращите и сорбционни свойства на активни въглени при приготвяне на вода от повърхностен източник // Вода, която пием: Резюмета на Международната научно -техническа конференция, Москва, 1-4 март 1995 г. - М. - 1995. - S 80-81.
- Клячков В. А., Апелцин И. Е. Пречистване на естествени води. - М.: Стройиздат, 1971.- 579 с.
- Чън Джи-гян, Уен Цин-сюе, Ли Бинг-нан. Подготовка на водата в процеса на непрекъсната филтрация // Harbin shangye Daxue xuebao ziran kexue ban. J. Harbin Univ. Commer. Натур. Sci. Ed. 2004. - 20, No 4. - P 425- 428.437.
- D? Bonski Zygmunt, Okoniewska Ewa. Wykorzystanie w? Gla aktywnego do usuwania manganu z wody // Uzdatn., Odnowa і wod: Konf. Politechn Czest., Czestochowa -Ustron, 4-6 marca, 1998. - Czestochowa, 1998 - P 33 - 37.
- Тютюнников Ю.Б., Посалевич М.И. Производство на сулфонирани въглища, подходящи за пречистване на питейна вода // Кокс и химия. - 1996. - No 12. - С. 31-33.
- Рождов И.И., Черкесов А.Ю., Рождов И.Н. Приложение на различни видове филтриращи среди в пречиствателни станции за обезглаждане // "TECHNOVOD - 2004" (технологии за пречистване на вода). Научни и практически материали. конференция, посветена на 100 -годишнината на SRSTU (NPI), Новочеркаск, 5 - 8 октомври 2004 г. - Новочеркаск: Издателство на НПО "ТЕМП". - 2004.- С. 70-74.
- Стрелко Владимир (младши), Малик датски Й., Стрийт Майкъл. Интерпретация на поведението на сорбция на преходни метали от окислени активни въглеродни атоми и други адсорбенти // Se-par Sci. и Технол. - 2004. - 39, No 8. - Р. 1885-1905.
- Татяна Савкина. Нанотехнологии за изпълнение на програмата "чиста вода". // Общинска Русия. Град Тюмен. - 2009. - 73 - 74, No 1 - 2. - С. 44-47.
- Лукашевич О. Д., Усова Н. Т. Изследване на адсорбционните свойства на шунгитовите филтриращи материали // Вода и екология. - 2004.- No 3.- С. 10-17.
- Журба М.Г., Вдовин Ю.И., Говорова Ж.М., Пушкин И.А. Съоръжения и устройства за прием и пречистване на вода Под. изд. М.Г. Журба.- М.: ИК „Астрел“, 2003.- 569s.
- Аюкаев Р.И., Мелцер В.З. Производство и използване на филтриращи материали за пречистване на водата. Л.: Стройиздат, 1985. - 120 -те.
- Лурие Ю.Ю. Аналитична химия на промишлени отпадни води. М.: Химия, 1984.- 447s.
- Потупване. 2060817 Русия MKI6 B 01 J 20/30, B 01 J 20/02/Господинов Д.Г., Пронин В.А., Шкарин А.В. // Метод за модифициране на естествен шунгитов сорбент. Новосибирски научен и инженерен център по екология на Министерството на железниците на Руската федерация. - Публ. 27.05.96, Бул. No15.
- Драгункина О.С., Мерзлякова О.Ю., Ромаденкина С.Б., Решетов В.А. Сорбционни свойства на шисти при контакт с нефт и водни разтвори на соли на тежки метали // (Саратовски държавен университет на името на Н. Г. Чернишевски, Саратов, Русия). Екология и научно-технически прогрес: Материали 3 международни научно-практически. conf. студенти, аспиранти и млади учени. - Перм: издателство Перм. състояние тези. не-това. - 2005.- С. 52 -54.
- Тарасевич Ю.И., Овчаренко Ф.Д. Адсорбция върху глинести минерали. -Киев: Наук. Думка, 1975.- 352 с.
- Тарасевич Ю.И. Естествени сорбенти в процесите на пречистване на водата.- Киев: Наук. Думка, 1981.-208 с.
- Тарасевич Ю.И. Структурата и химията на повърхността на слоести силикати.-Киев: Наук. Думка, 1988. - 248 с.
- Клячко В. А., Апелцин И. Е. Пречистване на естествени води. Москва: Стройиздат, 1971.- 579 с.
- Чернавина Т.Н., Антонова Е.Л. Модифицирани алумосиликатни сорбенти // Проблемен теор. и експерт. химия: Резюмета на 15 руски студ. научни. Conf., Посветена на 85 -годишнината на Уралския държавен университет. тях. A.M. Горки, Екатеринбург, 19 - 22 април 2005 г. - Екатеринбург: Издателство на Уралския държавен университет, 2005. - С. 145-146.
- Горова А.Н. Лапицки В.Н., Боцман Е.И. Перспективи за използването на естествени силикати в процеса на пречистване на отпадъчни води // Теория и практическа металургия. - 2004. - No 5. -S. 134-138.
- Потупване. 2263535 Русия, IPC 7 B 01 J 20/06, 20/16/Шафит Я. М., Солнцев В. В., Старицина Г. И., Ромашкин А. В., Шувалов В. И .. АД „Проект.- дизайн. фирма "Adsorber" // Сорбентен катализатор за пречистване на вода от манган. - Публ. 10.11.2005 г.
- Потупване. 2174871 Русия, MPK7 B 01 J 20/24 / Kertman S.V., Khritokhin N.A., Kryuchkova O.L. // Композитен хумоалуминосиликатен сорбент. - Публ. 20.10.2001 г.
- Куприенко П.Н. Използването на глинести минерали в технологията за пречистване на отпадъчни води // Вода и Водоч. технология. - 2005. - No2. - С. 41-45.
- Миронюк И.Ф. Промяна на микровискозитета на водата и за контакт с модифициран силициев диоксид // Допълнение. Национална академия на науките на Украйна. - 1999. - No4. - С. 86 -91.
- Машкова С.А., Разов В.И., Тонких И.В., Жамская Н.Н., Шапкин Н.П., Скобун А.С. Химическа модификация на вермикулит с хитозанферо-ферицианиден комплекс // Известия вузов. Химия и химия. технология. - 2005. - 48, No 6. - С. 149-152.
- Баротов М. А. Киселинно разлагане на цеолити на Таджикистан / Автореферат. дисертация за уч. Изкуство. Канд. технология Науки // Душанбе - 2006. - 22 с.
- Патент на САЩ 6921732, IPC7 B 01 J 29/06, NPK 502/66/ChK Group, Inc. Vempati Rajan K. No 10/796626 // Метод за производство на покрит цеолитен адсорбент. - Публ. 07.2005 г.
- Хасанов М.А. Адсорбционно пречистване на артезианска вода от желязо и манган с помощта на електрически разряди // Polzunovskiy Alm. - 2004. - No 4. - P.221-22z.
- Максимова Т.Н., Лаврухина Ю.А., Скворцова Н.В. Корекция на качеството на питейната вода в райони с проблемна екология // Трудове на Международното изложение научно -технически. conf. "Наука и образование" Мурманск: Издателство на МГТУ 2004. - с. 258-260.
- Tlupov R.M., Ilyin A.I., Shesterin I.S., Shakhmurzov M.N. Естествени зеолити - адсорбенти на токсични вещества в риболова // Вестник вет. - 1997. - No1. - С. 80-88.
- Скитър Н.А. Естествени и модифицирани сорбенти за деманганиране и обезвъздушаване на подземните води // Автореф. dis. за работа. ъч. Изкуство. Канд. технология Науки. - Новосибирск, - 2004. - 25 с.
- Skeeter N.A., Kondrova S.E. Нов естествен сорбент за извличане на тежки метали от водни среди // Int. научни и практически. conf. „Проблеми на инженерната поддръжка и екологията на градовете“, Пенза. Декември 1999 г .: Събиране на материали. Пенза: Издателство на Приволжския дом на знанието. - 1999. - С. 12-15.
- Bochkarev GR., Pushkareva GN., Skeeter N.A. Модифициран бруцит за деманганиране и обезвъздушаване на подземните води // Известия вузов. - 2001. - No 9 - 10. - С. 90 -94.
- Бобилева С.А. Сорбционно третиране на отпадъчни води от йони на тежки метали с помощта на бруцит // Резюме на дис. да кандидатства за академична ул. Кандидат на техническите науки. - 2005.- 24стр.
- Поляков В.Е., Полякова И.Г., Тарасевич Ю.И. Пречистване на артезианска вода от йони на манган и желязо с помощта на модифициран клиноптиломит // Химия и технология на водата. - 1997.19, № 5. - P.493-505.
- Николадзе Г.И., Минц Д.М., Касталски А.А. Подготовка на вода за питейно и промишлено водоснабдяване. - М.: Висше училище, 1984.- 368 с.
- Lubochnikov N.T., Pravdin E.P. Опитът с обезгладяването на питейна вода в Урал // Научни трудове „Водоснабжение” .- 52, № 5. - 1969. - S.103-106.
- Драхлин Е.Е. Пречистване на водата от желязо и манган чрез катионизация // Научни трудове "Водоснабдяване" - Брой 52, No 5. ОНТИАХ, 1969 г.-стр. 107-112.
- Потупване. Русия 2162737, MKI B 01 J20/02, 20/06, 20/30, B 01D 39/02/Дудин Д.В., Бодягин Б.О., Бодягин А.О. // Метод за получаване на гранулиран филтриращ материал - Публ. 10.02.2001 г.
- Кулски Л.А., Булава М.Н. Гороновски И.Т., Смирнов П.И. Проектиране и изчисление на пречиствателни съоръжения за водоснабдяване - Киев. Държавно строително издателство на Украинската ССР, 1961.- 353 с.
- Потупване. 49-30958 Япония. CO2B1 1/14 / - Публ. 17.08.74.
- Губайдулина Т. А., Почуев Н. А., Губайдулина Т. А. Филтриращ материал за пречистване на вода от манган и желязо, метод за неговото производство и метод за пречистване на вода от манган и желязо // Екол. системи и устройства. -2006.- No 8.- С. 59-61.
- Потупване. 2184708 Русия, MPK7 C 02 F 1/64 / Bochkarev G.R., Beloborodov A.V., Pushkareva G.N., Skiter N.A. // Метод за отстраняване на манган. - Публ. 07.2002 г.
- Заявка 2772019 Франция, IPC6 C 02 F 1/58 / Jauf -fret H. // Procede de deferrisation des eaux minerales ferrugineuses riches en gaz carbonique. - Публ. 06,99.
- Потупване. 95113534/25 Русия, MPK6 B 01 J20 / 05 / Леонтьева Г.В .; Волхин В.В .; Бахирева О.И. // Неорганичен йонообменник на базата на манганови оксиди () и метод за неговото производство. - Публ. 1997.08.20.
- Пушкарева Г.Н., Скитър Н.А. Възможност за използване на манганови руди при пречистване на водата // Физико -технически проблеми на разработването на полезни минерали. - 2002. - No 6. - S.103-107.
- Akdolit GmbH & Co. КИЛОГРАМА. N 102004049020.1; Appl. 10/05/2004; Публ. 06.04.2006г.
- Bitozor S., Llecki W, Raczyk-Stanislawia K.U., Nawrocki J. Jednoczesne usuwanie zwiaxk? W manganu i azotu amonowego z wody na zto? U piroluzytowym // Ochr. srod. - 1995. - No 4. - С. 13-18.
- Катаргина О.В., Бахирева О.И., Волхин В.В. Синтезни и сорбционни свойства на йонообменните материали на базата на смесени метални оксиди. // Резюмета на регионалната конференция. студенти и млади учени, Перм, 2003.: Издателство на Перм. държавен технически университет. - 2003.- С.64- 65.
- Pat 2226511 Русия, MPK7 C 02 F 1/64, 1/72, C 02 F 103/04/Bochkarev GR, Beloborodov A.V., Pushkareva GI., Skeeter // Метод за пречистване на водата от манган и/или желязо.- Публ. 04/10/2004.
- Стефаняк, Б. Билиш Ски б, Р. Доброволски в, П. Стащук д, Й. У? Джик. Колоиди и повърхности A: Физикохимични и инженерни аспекти, 2002, 208, стр. 337-345, Влиянието на условията за получаване върху адсорбционните свойства и порьозността на сорбенти на основата на доломит.
- C. Sistrnk, M.K. Рос, Н. М. Филипов Директен ефект на манганови съединения върху допамина и неговия метаболит Dopac: An in vitro стадия // Environmental Teicology fnd Pharmacology-2007.- 23.- P286-296.
- Курдюмов С.С., Брун-Цеховой А.Р., Паренаго О.П. Промени в структурните и физико -химичните свойства на доломита по време на разрушаването му при хидротермални условия // J. Phys. химия. - 2001. - 75, No10. - С. 1891-1894.
- Mamchenko A.V., Kiy N.N., Chernova L.G., Misochka I.M. Изследване на влиянието на методите за модифициране на естествени доломити върху деманганирането на водата // Химия и технология на водата. - 2008.- Т30, No 4.- С.347- 357
- Николенко. N.V., Kuprin V.P., Kovalenko I.L., Plaksienko I.L., Dovban L.V. Адсорбция на органични съединения върху калциеви и манганови карбонати // J. Phys. химия. - 1997. - 71, No 10. - С. 1838 -1843.
- А. Ю. Годимчук, А. П. Илин Изследване на сорбционните процеси върху естествени минерали и техните термично модифицирани форми // Химия и технология на водата. - 2004. - 26, бр.3. - С. 287-298.
- Илин А.П., Годимчук А.Ю. Изследване на процесите на пречистване на водата от тежки метали върху естествени минерали // Материали от доклади на 6-та Всеруска научно-техническа конференция „Енергия: екология, надеждност, безопасност“, Томск, 6-8 декември 2000 г. Т. Томск: Издателство ТПУ - 2000. - С. 256 - 257.
- Потупване. 2162737 Русия MPK7 B01J 20/02 / Дудин Д.В., Бодягин Б.О., Бодягин А.О // Метод за получаване на гранулиран филтриращ материал. - Публ. 02/10/2001.
- А. А. Седова, А. К. Осипов 24 Огарев. Дефлуориране на питейна вода с естествени сорбенти // Тез. доклад научни. Conf., Саранск, 4 - 9 дек. 1995. Част 3. Саранск, 1995.- С. 38- 39.
- Патент 84108 Украйна, IPC B01J 20/02, C02F 1/64/Гончарук В.В., Мамченко О.В., Кий М.М., Чернова Л.Г., Мисочка И.В. // Как да се отървем и как да се отървем от вода за почистване на вода от манган. - 09.2008.
- Потупване. 6596182 САЩ, IPC7 C 02 F 1/00, C 02 F 1/48/Prenger Coyne F, Hill Dallas D., Padilla Dennis D., Wingo Robert M., Worl Laura A., Johnson Michael D. // Магнитен процес за отстраняване на тежки метали от вода, използващи магнетити. - Публ. 22 юли 2003 г.
- В.В. Гончарук, В.М. Радовенчик, М.Д. Гомел. Otrimannya, че vicorystannya на силно разпръснати сорбенти с магнитни сили. - Киев: Вид., 2003. - 263 с.
При използване на вода от кладенец понякога се забелязва появата на тъмни зърна. Естествено възниква въпросът дали това може да бъде вредно за здравето и какво да се прави в тази ситуация.
Какво да направите, ако във водата се появят черни или сиви зърна?
Появата на забележими зърна във водата, необичайна миризма и обезцветяване са сигнал за наличието на вредни примеси. Ето защо, на първо място, е необходимо да се намали количеството на използваната вода до минимум и да се извърши анализ. Можете да го направите в частна лаборатория или санитарна станция. В зависимост от вида на анализа, резултатът ще трябва да изчака 3-7 дни.
Черно-сивите зърна във вода най-често сигнализират, че допустимото ниво на манган в нея е надвишено. В питейната вода този показател не трябва да надвишава 0,1 mg / l. В подземните източници този метал придружава желязото и е сходен по свойства с него.
Как манганът влияе на човешкото тяло
За човешкото здраве превишаването на концентрацията на манган е вредно. В допълнение към черно-сивите зърна, индикатор за повишено съдържание на манган е слаб жълт оттенък на вода и неприятен послевкус. Освен това последното се забелязва и в чая или кафето, а не само в непречистената вода. Основният отрицателен ефект на водата с високо съдържание на калций е върху нервната система. Според научни изследвания децата, които редовно използват високи дози манган, имат намалени интелектуални способности.
Също така вредното въздействие на мангана е и върху други органи. Например този елемент се обработва и съхранява от черния дроб, което се отразява на работата му. Манганът прониква в костите, червата, бъбреците и мозъка. Ако не предотвратите приема на манган в организма във високи дози, това в крайна сметка ще доведе до отравяне. Основните симптоми са:
- Срив и апатия;
- Замайване и главоболие;
- Намален апетит
- Постоянни промени в настроението;
- Болки в гърба и спазми.
Отоплителната система и водопроводите също са засегнати отрицателно. На повърхността им се образува плака, която възпрепятства преминаването на водния поток. С течение на времето плаката започва да се лющи. Те се появяват във водата под формата на зърна.
Какво да направите, ако концентрацията на манган във водата се увеличи
Поради вредното въздействие на мангана върху човешкото здраве е важно да се подхожда отговорно към пречистването на водата. Подходящото оборудване се избира въз основа на резултатите от анализа. Техният принцип на действие се основава на окисляването на манган. Поради това се утаява, което след това се отстранява механично.
Пречистваме водата от манган, филтри и цени Перм
| Име | Производителност m3 / h | Гаранция | Избор | Цена | Промоционална цена -30% |
|---|---|---|---|---|---|
| Омекотител WS 0844 | 0,6 | 5 години | Е свободен | 28 670 | 22 054 |
| Омекотител WS 1044 | 1,1 | 5 години | Е свободен | 35 411 | 27 239 |
| Омекотител WS 1054 | 1,5 | 5 години | Е свободен | 39 536 | 30 412 |
| Омекотител WS 12 | 1,8 | 5 години | Е свободен | 46 128 | 35 483 |
| Омекотител WS 13 | 2,1 | 5 години | Е свободен | 51 222 | 39 401 |
| Омекотител WS 14 | 2,8 | 5 години | Е свободен | 67 822 | 52 171 |