"... - Hvor mange papegøyer passer i deg, en slik økning.
- Virkelig trengte! Jeg vil ikke svelge så mange papegøyer! "
Fra m / f "38 papegøyer"
I samsvar med de internasjonale reglene i C (internasjonalt system av måleenheter), måles antall termisk energi eller mengden varme i Joules [J], det er også flere kilodzhuleenheter [KJ] \u003d 1000 J., Meghadzhoule [MJ] \u003d 1 000 000 J, Gigajoule [GJ] \u003d 1 000 000 000 J., etc. Denne enheten for måling av termisk energi er den viktigste internasjonale enheten og brukes oftest når de utfører vitenskapelige og vitenskapelige og tekniske beregninger.
Men vi alle vet eller i det minste en gang hørt en annen måleenhet av mengden varme (eller bare varme) en kalori, så vel som kilocaloria, megaklorin og gigangloria, som betyr CILO, GIGA og MEGA-konsoller, se et eksempel med joules ovenfor. I vårt land, historisk utviklet på en slik måte at når man beregner oppvarmingstariffer, er det oppvarming av elektrisitet, gass- eller pelletskjeler, det er vanlig å vurdere kostnaden for nøyaktig ett gigapporin av termisk energi.
Så hva er gigappor, kilowatt, kilowatt * en time eller kilowatt / time og jouli, og hvordan er de relatert til hverandre ?, Du vil lære i denne artikkelen.
Så, hovedenheten av termisk energi er, som allerede nevnt, Joule. Men før du snakker om måleenhetene, er det i prinsippet i prinsippet på husstandsnivået for å avklare hva slags termisk energi er og hvordan og hva du skal måle den.
Vi kjenner hele barndommen din for å varme opp (få varme) Du må sette opp noe, så vi alle brente branner, tradisjonelt drivstoff for brannen er et ved. Således, åpenbart, når det brenner brennstoffet (noen: brensel, kull, pellets, naturgass, diesel), er termisk energi (varme) skilt. Men for å varme, for eksempel, krever forskjellige volumer vann en annen mengde brensel (eller annet drivstoff). Det er klart at for å varme to liter vann, flere fives i brannen, og å forberede en halv suppe til hele leiren, må du fylle opp med flere knittere av brensel. For ikke å måle slike strenge tekniske verdier som mengden varme- og varmeforbrenning av drivstoff med brensel av brensel og skuldre med suppe, besluttet varmeingeniører å gjøre klarhet og orden og enige om å oppfinne en enhet av mengden varme. Slik at denne enheten var overalt. Det samme bestemte det: å varme en kilo vann i en grad under normale forhold (atmosfærisk trykk), er 4,190 kalorier nødvendig, eller 4,19 kokaloria, derfor for å varme en gram vann vil være ganske tusen ganger mindre varme - 4,19 kalorier.
Kalorie er knyttet til den internasjonale enheten av termisk energi - Joule følgende forhold:
1 Calorie \u003d 4.19 Joule.
Således, for oppvarming 1 gram vann i en grad, vil 4,19 Joule av termisk energi være nødvendig, og for oppvarming ett kilo vann 4 190 joule varme.
I teknikken, sammen med en måling av termisk (og annen) energi, er det en kraftenhet og i samsvar med det internasjonale systemet (C), er dette watt. Konseptet med makt gjelder også for oppvarmingsenheter. Hvis oppvarmingsanordningen er i stand til å gi 1 sekund til 1 Joule termisk energi om 1 sekund, så er strømmen 1 watt. Makt, dette er evnen til å produsere (skape) en viss mengde energi (i vårt tilfelle av termisk energi) per tidsenhet. La oss gå tilbake til vårt eksempel med vann for å varme en kilo (eller en liter, i tilfelle av et kilo vann er lik liter) vann i en grad Celsius (eller Celvin, uten forskjell), vil vi trenge 1 cywlolarium-kraft eller 4,130 J. Varmeenergi. For å varme ett kilo vann i 1 sekund for 1 Cruds, trenger vi enheten neste kraft:
4190 J. / 1 \u200b\u200bS. \u003d 4 190 W. eller 4,19 kW.
Hvis vi ønsker å varme vår kilo vann i 25 grader i samme sekund, trenger vi kraft hver tjuefem ganger mer enn.
4,19 * 25 \u003d 104,75 kW.
Dermed kan det konkluderes med at en pellet kjele med en kapasitet på 104,75 kW. Varmes 1 liter vann med 25 grader på ett sekund.
Siden vi kom til Watt og Kilowatt, bør du også kaste et ord om dem. Som watt allerede er sagt - dette er en kraft enhet, inkludert kjelen, men i tillegg til pellet kjeler og gasskjeler, er menneskeheten kjente og elektrocotels, hvor kapasiteten måles, selvfølgelig, i samme kilowatts Og de forbruker ikke pellets og ikke gass, og elektrisitet, hvorav mengden måles i kilowatt timer. Riktig stavemåte av enheten av Energy Kilowatt * time (det er Kilowatt multiplisert i en time, ikke delt), opptak av kw / time - er en feil!
I elektrodukt blir elektrisk energi omgjort til termisk (såkalt, jowlevo varme), og hvis kjelen forbruker 1 kW * time elektrisitet, hvor mye fungerte det med varme? For å svare på dette enkle spørsmålet, må du utføre en enkel beregning.
Vi forvandler kilowatt til Kilodzhoule / sekunder (Kilodzhoule per sekund), og timer per sekund: på en time 3.600 sekunder, får vi:
1 kW * Time \u003d [1 KJ / S] * 3600 c. \u003d 1 000 J * 3600 C \u003d 3 600 000 Joule eller 3,6 MJ.
Så,
1 kW * time \u003d 3,6 mJ.
I sin tur, 3,6 MJ / 4,19 \u003d 0,859 μAL \u003d 859 kcal \u003d 859 000 avføring. Energi (termisk).
La oss nå vende seg til Gigapporia, hvis pris på ulike typer drivstoff er som å vurdere varmeteknikk.
1 GCAL \u003d 1 000 000 000 KAL.
1 000 000 000 Kal. \u003d 4.19 * 1 000 000 000 \u003d 4 190 000 000 J. \u003d 4 190 MJ. \u003d 4.19 GJ.
Eller å vite at 1 kW * time \u003d 3,6 MJ, beregner vi 1 gigaklora på Kilowatt * Watch:
1 GCAL \u003d 4190 MJ / 3,6 MJ \u003d 1 163 kW * timer!
Hvis du har lest denne artikkelen, bestemmer du deg for å konsultere en spesialist i vårt firma på ethvert problem relatert til varmeforsyning, så Her!
Kilde: teplo-en.ru.
(eller varmeoverføring).
Spesifikk varmekapasitet på stoffet.
Varmekapasitet - Dette er mengden varme som absorberes av kroppen når den er oppvarmet med 1 grad.
Kropps varmekapasitet er indikert av tittelen latinbrevet FRA.
Hva avhenger av kroppskapasiteten til kroppen? Først av alt, fra sin masse. Det er klart at for oppvarming, for eksempel, vil 1 kilo vann trenge mer varme enn for oppvarming 200 gram.
Og fra den slags stoff? Vi opplever. Ta to identiske fartøyer, og i en av dem veier vann 400, og i den andre - vegetabilsk olje som veier 400 g, begynner vi å varme dem med samme brenner. Ser på vitnesbyrd om termometre, vil vi se at oljen varmes opp raskt. For å varme vannet og oljen til samme temperatur, skal vann oppvarmes lenger. Men jo lenger vi oppvarmet vannet, desto større er mengden varme det kommer fra brenneren.
Således, for oppvarming av samme masse av forskjellige stoffer opp til samme temperatur, er det nødvendig med en annen mengde varme. Mengden varme som kreves for å varme opp kroppen, og derfor er varmekapasiteten avhengig av hvilken type stoff som dette organet består av.
For eksempel, for å øke med 1 ° C vanntemperatur som veier 1 kg, er mengden varme nødvendig, lik 4200 J, og for oppvarming med 1 ° C av samme masse av solsikkeolje, mengden varme som er lik 1700 j .
Den fysiske verdien som viser hvor mye varme som kreves for oppvarming 1 kg substans per 1 ºС, kalt spesifikk varme Dette stoffet.
Hvert stoff har sin egen spesifikke varme, som er indikert av latinbrevet C og måles i joules per kilo-grad (J / (kg ° C)).
Den spesifikke varmekapasiteten på samme substans i forskjellige aggregatstater (fast, flytende og gassformig) er forskjellig. For eksempel er den spesifikke vannkapasiteten til vann 4200 j / (kg · ºс, og isens spesifikke varmekapasitet er 2100 J / (kg ° C); Aluminium i en fast tilstand har en spesifikk varmekapasitet som er lik 920 J / (kg ° C), og i flytende - 1080 J / (kg-° C).
Legg merke til at vann har en svært større spesifikk varmekapasitet. Derfor, vann i havene og havene, oppvarming om sommeren, absorberer en stor mengde varme fra luften. På grunn av dette, på de stedene som ligger i nærheten av de store vannkroppene, er sommeren ikke så varm, både på steder fjernet fra vannet.
Beregning av mengden varme som kreves for å varme opp kroppen eller avkjølingen tildelt av den.
Det er klart fra det ovennevnte at mengden varme som kreves for oppvarming av kroppen, avhenger av hvilken type stoff hvorfra kroppen består (dvs. dens spesifikke varme), og fra kroppsvekt. Det er også klart at mengden varme avhenger av hvor mye grader vi skal øke kroppstemperaturen.
Så, for å bestemme mengden varme som kreves for oppvarming av kroppen eller avkjølingen som er tildelt den under avkjøling, blir den spesifikke varmekapasiteten til kroppen multiplisert med sin masse og forskjellen mellom dens endelige og innledende temperaturer:
Q. = cm. (t. 2 - t. 1 ) ,
hvor Q. - Mengde varme, c. - spesifikk varme, m. - kroppsmasse , t. 1 - Initial tempo, t. 2 - Enfinitiv temperatur.
Ved oppvarming av kroppen t 2\u003e t. 1 Og derfor, Q. > 0 . Når du kjøper kroppen t 2.< t. 1 Og derfor, Q.< 0 .
I tilfelle varmekapasiteten til hele kroppen er kjent FRA, Q. Bestemt av formelen:
Q \u003d c (t 2 - t. 1 ) .
Per definisjon er kalorier mengden varme som kreves for å varme en enkelt kubisk centimeter vann til 1 grader Celsius. Gigaklorin brukes til å måle termisk energi i termisk kraft og verktøy er en milliard kalorier. I 1 meter, 100 centimeter, derfor i en kubikkmeter - 100 x 100 x 100 \u003d 1000000 centimeter. Så å varme vannkuben på
1 grader, det vil ta en million kalori eller 0,001 GCAL.
I min by er oppvarmingsprisen $ 1132,22 / GKAL, og prisen på varmt vann - 71,65 rubler / kubikkmeter, prisen på kaldt vann er 16,77 rubler / kubikkmeter.
Hvor mange GKAL blir brukt til å varme 1 kube vann?
jeg tror det
s x 1132,22 \u003d 71,65 - 16,77 og dermed løser ligningene for å finne ut hva som er lik S (GCAL), det vil si, er 0,0484711452 GCAL
Jeg tviler på noe, etter min mening, jeg vil ikke bestemme
SVAR:
Jeg finner ikke feil i beregningen din.
Naturligvis bør kostnaden for avløpsvann (drenering) ikke være tilstede i de ovennevnte takstene.
Den omtrentlige beregningen i Izhevsk på gamle standarder ser slik ut:
0,19 GCAL per person per måned (denne hastigheten er nå kansellert, men den andre er for eksempel ikke egnet) / 3,6 kubikkmeter. per person per måned (forbrukshastigheten av varmt vann) \u003d 0,05278 GCAL per 1 kubikkmeter. (Så mye trenger varme for oppvarming 1 kubikkmeter. Kaldt vann til den normative temperaturen på varmt vann, som minner om, er 60 grader. C).
For en mer nøyaktig beregning av mengden termisk energi for å varme opp vannet ved direkte metode på grunnlag av fysiske mengder (og ikke tilbake gjennom de godkjente tariffene for DHW) - jeg anbefaler å bruke mal for beregning av tariff for varmt vann (REC). Beregningsformelen, blant annet bruker temperaturen på kaldt vann om sommeren og vinteren (oppvarming) perioder, varigheten av disse periodene.
Tags: gigakloria, varmt vann
- Vi betaler for GWS-tjenestene, temperaturen er betydelig lavere enn standarden. Hva å gjøre?
- Til slutt etablert av reglene, er nedleggelsen av DHW ikke ulovlig - beslutningen fra Høyesterett i Russland (2017)
- Initiativ for å etablere mer rettferdige tariffer og metoder for varmtvannsforbruk
- På prosedyren for å omregne størrelsen på ladningen for oppvarming og varmtvann under nedleggelse - avklaring av Rospotrebnadzor for UR
- På regnskapsføring av kjølevæsken i et lukket varmeforsyningssystem - et brev i departementet for interne saker i den russiske føderasjonen på 31.03.2015 nr. 9116-OD / 04
- Ur - om å redusere kostnadene for oppvarming og DHW - Brev av departementet for energien til ur til 08/17/2015 №11-10 / 5661
- Hva er det normative termen for verifiseringen av en generell vennlig måling av oppvarming og DHW?
- Skitten varmt vann fra under springen. Hvor skal du kontakte?
- Kan vannmåleren i leiligheten sette den for hele inngangen? Hvordan betale? Indikasjoner for måneden - 42 kubikkmeter
- Prosedyren for å opprettholde en separat regnskapsføring av kostnader innen vannforsyning og drenering - rekkefølgen av undervisningsministeren til den russiske føderasjonen 25. januar 2014 №22 /
- avgift for vann og elektrisitet i leiligheten uten overnatting
- beregning av varme i OTP 1/12
- Strømforsyning
- Store betalinger for rommet på vandrerhjemmet (17,3 kvm)
| Kommentarer: (11) | |
| Tips: Del en lenke i sosiale nettverk, hvis du vil få flere svar / kommentarer! | |
730. Hvorfor brukes vann til å kjøle noen mekanismer?
Vann har en stor spesifikk varmekapasitet, noe som bidrar til en god varmefjerning fra mekanismen.
731. I så fall må du bruke mer energi: for oppvarming ved 1 ° C av en liter vann eller for oppvarming ved 1 ° C. Ett hundre gram vann?
Å varme liter vann, som den større massen, jo mer energi du trenger.
732. Melchive og sølvplugger av samme masse senket varmt vann. Får de det samme vannet for å få det samme vannet?
Melchiorgaffel vil motta mer varme, fordi den spesifikke varmekapasiteten til melchior er større enn sølv.
733. På et stykke bly og på et stykke støpejern ble den samme massen rammet av en sledehammer. Hvilket stykke var vanskeligere?
Ledelsen varmer opp sterkere, fordi dens spesifikke varmekapasitet er mindre enn støpejern, og for oppvarming er det nødvendig med mindre energi.
734. I en kolbe er det vann, i den andre - kerosen av samme masse og temperatur. Hver kolbe ble kastet på samme oppvarmede jernkub. Hva er oppvarmet til høyere temperatur - vann eller parafin?
Kerosen.
735. Hvorfor i byene på kysten av temperaturfluktuasjoner om vinteren og sommeren mindre kutting enn i byene som ligger i dypet av fastlandet?
Vann varmer opp og avkjøler langsommere enn luft. Om vinteren kjøler den og beveger den varme massen av luft til landet, noe som gjør klimaet på kysten varmere.
736. Aluminiums spesifikke varmekapasitet er 920 j / kg ° C. Hva betyr dette?
Dette betyr at for oppvarming 1 kg aluminium ved 1 ° C er det nødvendig å bruke 920 J.
737. Aluminium og kobberstenger med samme masse på 1 kg avkjøles ved 1 ° C. Hvor mye vil den interne energien endre hver bar? Hvilken bar endrer den mer og hvor mye?
738. Hvilken mengde varme er nødvendig for å varme kilo-jernbanet til 45 ° C?
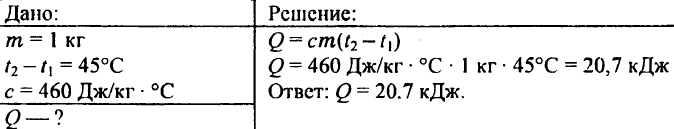
739. Hvilken mengde varme er nødvendig for å varme 0,25 kg vann fra 30 ° C til 50 ° C?
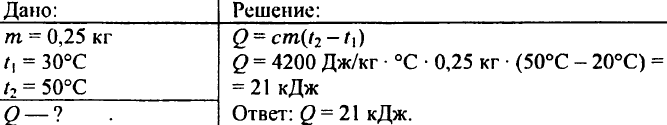
740. Hvordan vil den indre energien endres to liter vann når de oppvarmes ved 5 ° C?

741. Hvilken mengde varme er nødvendig for oppvarming av 5 g vann fra 20 ° C til 30 ° C?

742. Hvilken mengde varme er nødvendig for å varme opp aluminiumkulen med en masse på 0,03 kg ved 72 ° C?

743. Beregn mengden varme som kreves for oppvarming av 15 kg kobber ved 80 ° C.

744. Beregn mengden varme som kreves for oppvarming 5 kg kobber fra 10 ° C til 200 ° C.

745. Hvilken mengde varme er nødvendig for oppvarming 0,2 kg vann fra 15 ° C til 20 ° C?

746. Vann som veier 0,3 kg avkjølt ved 20 ° C. Hvor mye reduserte vannets indre energi?

747. Hvilken mengde varme må være 0,4 kg vann ved en temperatur på 20 ° C varme til en temperatur på 30 ° C?

748. Hvilken mengde varme blir brukt på oppvarming 2,5 kg vann ved 20 ° C?

749. Hvilken mengde varme som frigjøres ved avkjølt 250 g vann fra 90 ° C til 40 ° C?

750. Hvilken mengde varme må varme ved 1 ° C 0,015 l?
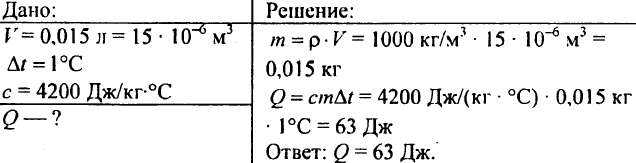
751. Beregn mengden varme som kreves for å varme inn 300 m3 dammen ved 10 ° C?

752. Hvilken mengde varme skal jeg vite 1 kg vann for å øke temperaturen fra 30 ° C til 40 ° C?

753. Vannet på 10 l avkjøles fra en temperatur på 100 ° C til en temperatur på 40 ° C. Hvilken mengde varme mediert på samme tid?

754. Beregn mengden varme som er nødvendig for oppvarming 1 m3 sand ved 60 ° C.

755. Luftvolumet er 60 m3, spesifikk varmekapasitet på 1000 j / kg ° C, lufttetthet er 1,29 kg / m3. Hvilken mengde varme er nødvendig for å varme den ved 22 ° C?

756. Vann oppvarmet ved 10 ° C, utgifter 4,20 103 J varme. Bestemme mengden vann.
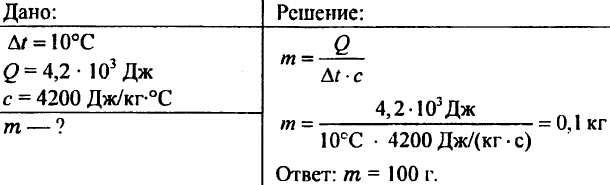
757. Vann som veier 0,5 kg ble rapportert til 20,95 KJ varme. Hva var vanntemperaturen, hvis den første vanntemperaturen var 20 ° C?

758. I en kobberpanne veier 2,5 kg, 8 kg vann ved 10 ° C. Hvilken mengde varme er nødvendig for vann i en kasserolle å koke?

759. En liter vann ved en temperatur på 15 ° C helles i en kobberbøtte som veier 300 g. Hvilken mengde varme er nødvendig for å varme vannet i bøtte ved 85 ° C?
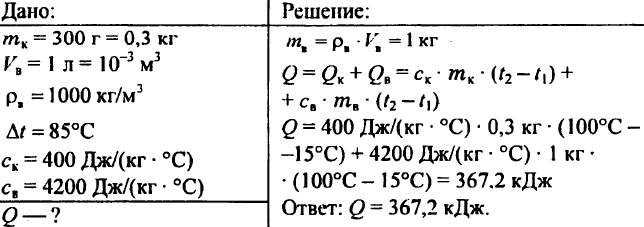
760. Et stykke oppvarmet granittvekt 3 kg er plassert i vann. Granitt overfører 12,6 kJ varmevann, avkjøling ved 10 ° C. Hva er den spesifikke varmekapasiteten til steinen?

761. Til 5 kg vann ved 12 ° C ble varmtvannet verdsatt ved 50 ° C, som har oppnådd en blanding med en temperatur på 30 ° C. Hvor mye vann festet?

762. I 3 liter vann ved 60 ° C ble vannet fylt ved 20 ° C, med oppnådd vann ved 40 ° C. Hvor mye vann festet?

763. Hva vil være temperaturen på blandingen, hvis du blander 600 g vann ved 80 ° C med 200 g vann ved 20 ° C?

764. En liter vann ved 90 ° C ble hellet i vann ved 10 ° C, og temperaturen på vannet var 60 ° C. Hvor mye kaldt vann var?

765. Bestem hvor mye det er nødvendig å helle varmt vann i et fartøy, oppvarmet til 60 ° C, hvis 20 liter kaldt vann allerede er i fartøyet ved 15 ° C; Temperaturen i blandingen skal være 40 ° C.
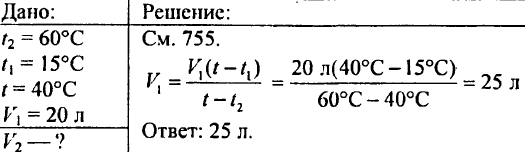
766. Bestem hvor mye varme som kreves for oppvarming av 425 g vann ved 20 ° C.

767. Hvor mye grader er 5 kg vann, hvis vannet får 167,2 kJ?

768. Hvor mye varme er nødvendig, slik at m av vann gram ved en temperatur T1, varme til temperatur T2?
769. I kalorimeteret helles 2 kg vann ved en temperatur på 15 ° C. Til hvilken temperatur oppvarmes av kalorimeterens vann, hvis det senkes i det en messing med 500 g, oppvarmet til 100 ° C? Spesifikk varmekapasitet på messing 0,37 KJ / (kg ° C).

770. Det er samme volum av stykker kobber, tinn og aluminium. Hvilke av disse stykkene har den største og hvilken laveste varmekapasitet?

771. Kalorimeteret ble hellet 450 g vann, hvor temperaturen er 20 ° C. Når 200 g jernsaggraver oppvarmet til 100 ° C ble lastet inn i dette vannet, var vanntemperaturen 24 ° C. Bestemme den spesifikke varmekapasiteten til sagflis.

772. Kobberkalorimeteret som veier 100 g, har plass til 738 g vann, hvor temperaturen er 15 ° C. Dette kalorimeteret ble senket 200 g kobber ved en temperatur på 100 ° C, hvorpå kalorimetertemperaturen steg til 17 ° C. Hva er den spesifikke varmekapasiteten til kobber?

773. Stålkulen veier 10 g fjernes fra ovnen og senkes i vann med en temperatur på 10 ° C. Vanntemperaturen steg til 25 ° C. Hva var temperaturen på ballen i ovnen, hvis vannmassen er 50 g? Den spesifikke varmekapasiteten til stålet er 0,5 kJ / (kg ° C).
776. Vann som veier 0,95 g ved en temperatur på 80 ° C ble blandet med vann som veier 0,15 g ved en temperatur på 15 ° C. Bestem temperaturen på blandingen. 779. Stålkutter som veier 2 kg ble oppvarmet til en temperatur på 800 ° C og deretter utelatt til et fartøy inneholdende 15 liter vann ved en temperatur på 10 ° C. Hvilken temperatur vil vannet bli oppvarmet i fartøyet?

(Merk. For å løse dette problemet er det nødvendig å gjøre en ligning der det ukjente vedtar den ønskede vanntemperaturen i fartøyet etter å ha senket kutteren.)
780. Hvilken temperatur er vann, hvis du blander 0,02 kg vann ved 15 ° C, 0,03 kg vann ved 25 ° C og 0,01 kg vann ved 60 ° C?

781. For oppvarming av en godt ventilert klasse, er mengden varme 4,19 mj per time. Vann går inn i varmejernene ved 80 ° C, og kommer ut av dem ved 72 ° C. Hvor mye vann skal serveres hver time i radiatorer?

782. Lead som veier 0,1 kg ved en temperatur på 100 ° C ble nedsenket i et aluminiumkalorimeter som veide 0,04 kg, inneholdende 0,24 kg vann ved 15 ° C. Deretter ble en temperatur på 16 ° C installert i kalorimeteret. Hva er den spesifikke blykvarmekapasiteten?

Mennesket kjenner noen typer energi - mekanisk energi (kinetisk og potensial), intern energi (termisk), feltenergi (gravitasjon, elektromagnetisk og kjernefysisk), kjemisk. Separat er det verdt å markere eksplosjonens energi, ...
Vakuum energi og til og med eksisterende bare i teorien - mørk energi. I denne artikkelen, først i overskriften "Varmteknikk", vil jeg prøve på et enkelt og tilgjengelig språk ved hjelp av et praktisk eksempel, for å fortelle om den viktigste form for energi i livet til mennesker - om termisk energi og om kjedelig det i tide termisk kraft.
Noen få ord for å forstå varmenes sted, som seksjonen av vitenskapen om å skaffe seg, overføre og bruke termisk energi. Moderne varmeteknikk har blitt skilt fra den generelle termodynamikken, som igjen er en av delene av fysikk. Termodynamikk er en bokstavelig "varm" pluss "kraft". Dermed er termodynamikk en vitenskap om "endring i temperatur" av systemet.
Påvirkningen på utsiden, hvor dens interne energi endres, kan være et resultat av varmeveksling. Termisk energisom er kjøpt eller tapt av systemet som følge av slik samhandling med miljøet, kalles mengde varme Og målt i SI-systemet i Joules.
Hvis du ikke er en ingeniør-varmeingeniør, og ikke hver dag, gjør du varmeknikkproblemer, så du står overfor dem, noen ganger uten erfaring, er det svært vanskelig å finne ut dem. Det er vanskelig uten nærvær av erfaring å presentere selv dimensjonen av de nødvendige verdiene av mengden varme og termisk kraft. Hvor mange Joule Energy er nødvendig for å varme 1000 meter kubisk luft fra temperatur -37˚с til + 18 ° C ?. Hva er kraften i varmekilden, for å gjøre det om 1 time? .. på disse ikke mest Vanskelige spørsmål er i stand til å svare i dag. "Ikke alle ingeniører. Noen ganger husker eksperter selv formelen, men bare enheter kan bruke dem i praksis!
Etter å ha lest denne artikkelen til slutten, kan du enkelt løse ekte produksjons- og husholdningsproblemer forbundet med oppvarming og avkjøling av ulike materialer. Å forstå den fysiske essensen av varmeoverføringsprosesser og kunnskap om enkle grunnleggende formler er de viktigste blokkene i grunnlaget for kunnskap om varmeteknikk!
Mengden varme i forskjellige fysiske prosesser.
De fleste av de kjente substansene kan være i faste, flytende, gassformige eller plasmapriser ved forskjellige temperaturer og trykk. Overgang fra en samlet tilstand til en annen skjer med en konstant temperatur (forutsatt at trykk og andre miljømessige parametere ikke endres) og ledsages av absorpsjon eller separasjon av termisk energi. Til tross for at i universet er 99% av stoffet i en tilstand av plasma, vi vil ikke vurdere dette aggregatet i denne artikkelen.
Vurder tidsplanen som presenteres i figuren. Det skildrer avhengigheten av temperaturen på stoffet T. Fra mengden varme Q. sendt til et bestemt lukket system som inneholder en viss masse av noe bestemt stoff.

1. Fast T1. , oppvarmet til temperatur Tpl. , utgifter på denne prosessen mengden varme som er lik Q1. .
2. Neste begynner smelteprosessen, som oppstår ved konstant temperatur. Tpl. (smeltepunkt). For å smelte hele massen av den faste kropp, er det nødvendig å bruke varmen i mengden termisk energi Q2. - Q1. .
3. Neste, væsken, oppnådd som et resultat av smelting av faststoff, oppvarmet til kokepunktet (gassdannelse) TKP. , utgifter på denne mengden varme lik Q3.-Q2. .
4. Nå på uendret kokepunkt TKP. Flytende kokes og fordamper, blir til gass. For å bytte hele massen av væske til gass, er det nødvendig å bruke termisk energi i mengden Q4.-Q3..
5. På den siste fasen er gass oppvarmet på temperatur TKP. Til noen temperatur T2. . I dette tilfellet vil kostnaden for mengden varme være Q5.-Q4. . (Hvis de er raske gass til ioniseringstemperaturen, vil gassen bli til et plasma.)
Således varmekilde fast stoff fra temperaturen T1. til temperatur T2. Vi brukte termisk energi i mengde Q5. , oversette stoffet gjennom tre aggregatstater.
Beveger seg i motsatt retning, vil vi tildele fra stoffet samme mengde varme Q5.Passerer trinnene for kondensering, krystallisering og kjøling fra temperatur T2. til temperatur T1. . Selvfølgelig vurderer vi et lukket system uten energitap til det ytre miljøet.
Merk at det er mulig å overgå fra en fast tilstand til en gassformig tilstand, omgå væskefasen. En slik prosess er referert til som sublimering, og omvendt prosess til den - desublimation.
Så forsto vi at overgangsprosessene mellom stoffets samlede tilstand er preget av energiforbruk ved konstant temperatur. Ved oppvarming av stoffet som befinner seg i en uendret aggregattilstand, blir temperaturen stiger og termisk energi også konsumert.
De viktigste formlene av varmeoverføring.
Formler er veldig enkle.
Mengde varme Q. I J, er det beregnet av formlene:
1. Fra forbruket av varme, det vil si, fra lastsiden:
1.1. Når oppvarmet (kjøling):
Q. = m. * c. * (T2 -t1)
m. – masse substans i kg
fra -spesifikk varmekapasitet på stoffet i j / (kg * k)
1.2. Når smelting (frysing):
Q. = m. * λ
λ – spesifikk varme smelting og krystallisering av materie i j / kg
1.3. Ved koking, fordampning (kondensering):
Q. = m. * r.
r. – spesifikk varme av gassdannelse og kondensering av materie i j / kg
2. Fra varmen av varme, det vil si, fra siden av kilden:
2.1. Ved forbrenning av drivstoff:
Q. = m. * q.
q. – spesifikk varmeforbrenning av drivstoff i j / kg
2.2. Ved transformering av elektrisitet til termisk energi (Jouleens lov - Lenza):
Q \u003d t * i * u \u003d t * r * i ^ 2 \u003d (t / R)* U ^ 2
t. – tid i S.
JEG. – aktiv verdi av strøm i a
U. – den aktive verdien av spenningen i
R. – last motstand i ohm
Vi konkluderer - mengden varme er direkte proporsjonal med massen av stoffet i alle fase transformasjoner og når oppvarmet er dessuten direkte i forhold til temperaturforskjellen. Proporsjonalitetskoeffisienter ( c. , λ , r. , q. ) For hvert stoff har de egne verdier og bestemmes av den eksperimentelle måten (tatt fra referansebøker).
Termisk kraft N. I W er dette mengden varme som overføres av systemet for en viss tid:
N \u003d q / t
Jo raskere vi ønsker å varme opp kroppen opp til en viss temperatur, desto større må kraften være kilden til termisk energi - alt er logisk.
Beregning i Excel-applikasjonsoppgaver.
I livet er det ofte nødvendig å foreta en rask evalueringsberegning for å forstå om det er fornuftig å fortsette å lære emnet, gjøre prosjektet og distribuere nøyaktige arbeidsintensive beregninger. Gjør en beregning om noen få minutter Selv med en nøyaktighet på ± 30%, kan du ta en viktig ledelsesløs løsning som vil være 100 ganger billigere og 1000 ganger mer operativt og som et resultat 100.000 ganger mer effektivt enn å utføre en nøyaktig beregning innen en uke , og da og måneden, en gruppe av dyre spesialister ...
Betingelser for problemet:
Til lokalene til verkstedet for utarbeidelsen av metall med dimensjoner på 24m x 15m x 7m bringer fra et lager på en metallvalsegate i mengden 3T. På metallet er det en is med en totalvekt på 20 kg. På gaten -37˚с. Hvor mye varme er nødvendig for å varme metallet til + 18 ° C; Varm isen, smelte den og varme vannet til + 18 ° C; Varm hele volumet av luft innendørs, forutsatt at før det var oppvarming helt deaktivert? Hvilken kraft skal ha varmesystemet, hvis alt ovenfor må være ferdig i 1 time? (Veldig tøff og nesten ingen reelle forhold - spesielt angående luft!)
Beregning vil bli utført i programmetMS Excel. eller i programmetOoo calc..
Med fargeformatering av celler og fonter, sjekk ut siden "".
Innledende data:
1. Navnene på stoffet skriver:
i D3-cellen: Stål
i Cell E3: Is
i celle F3: Isvann
i celle G3: Vann
i celle G3: Luft
2. Prosessnavn Vi introduserer:
i celler D4, E4, G4, G4: varme
i F4-cellen: smelting
3. Spesifikk varmekapasitet c. i j / (kg * k) skriver vi for henholdsvis stål, is, vann og luft
i D5-cellen: 460
i celle E5: 2110
i cellen G5: 4190
i Cell H5: 1005
4. Spesifikk varme av smelting is λ i j / kg passer
i Cell F6: 330000
5. Masse av stoffer m. I KG passer henholdsvis for stål og is
i D7-cellen: 3000
i celle E7: 20
Siden isen blir til vann, endres ikke massen,
i celler F7 og G7: \u003d E7 =20
Massen av luft finner vi produktet av rommet på andelen
i H7-cellen: \u003d 24 * 15 * 7 * 1,23 =3100
6. Tidsprosesser t. i min skrive bare en gang for stål
i D8-cellen: 60
Tiden for oppvarming av is, dens smelting og oppvarming av det resulterende vannet beregnes fra tilstanden at alle disse tre prosessene skal oppfylle i mengden av samme tid som metallet påføres oppvarming. Les henholdsvis
i Cell E8: \u003d E12 / (($ E $ 12 + $ F $ 12 + $ G $ 12) / D8) =9,7
i cellen F8: \u003d F12 / (($ E $ 12 + $ F $ 12 + $ g $ 12) / D8) =41,0
i cellen G8: \u003d G12 / (($ E $ 12 + $ F $ 12 + $ g $ 12) / d8) =9,4
Luft bør også varme opp for samme tildelte tid, lese
i H8-cellen: \u003d D8 =60,0
7. Innledende temperatur på alle stoffer T.1 I C Co.
i D9-cellen: -37
i celle E9: -37
i Cell F9: 0
i cellen G9: 0
i cellen H9: -37
8. Enfinitiv temperatur på alle stoffer T.2 I C Co.
i D10-cellen: 18
i celle E10: 0
i F10-cellen: 0
i cellen G10: 18
i celle H10: 18
Jeg tror spørsmål i henhold til s. 7 og punkt 8 være uferdig.

Resultater av beregninger:
9. Mengde varme Q. I KJ, som er nødvendig for hver av prosessene, forventer vi
for oppvarmingstål i D12-cellen: \u003d D7 * D5 * (D10-D9) / 1000 =75900
for isoppvarming i celle E12: \u003d E7 * E5 * (E10-E9) / 1000 = 1561
for smelting av is i celle F12: \u003d F7 * F6 / 1000 = 6600
Å varme vannet i cellen G12: \u003d G7 * G5 * (G10-G9) / 1000 = 1508
for luftoppvarming i H12-cellen: \u003d H7 * H5 * (H10-H9) / 1000 = 171330
Totalt antall termisk energi som kreves for alle prosesser som leses
i den kombinerte cellen D13E13F13G13H13: \u003d Sums (D12: H12) = 256900
I cellene D14, E14, F14, G14, H14 og den kombinerte cellen D15E15F15G15H15, er mengden varme gitt i en buemåling - i GCAL (i gigaktoria).
10. Termisk kraft N. I KW beregnes det nødvendige for hver av prosessene
for oppvarmingstål i cellen D16: \u003d D12 / (D8 * 60) =21,083
for isoppvarming i celle E16: \u003d E12 / (E8 * 60) = 2,686
for smelting av is i celle F16: \u003d F12 / (F8 * 60) = 2,686
Å varme vannet i cellen G16: \u003d G12 / (G8 * 60) = 2,686
for luftoppvarming i cellen H16: \u003d H12 / (H8 * 60) = 47,592
Total termisk kraft som kreves for å oppfylle alle prosesser i løpet av tiden t. regnet ut
i den kombinerte cellen D17E17F17G17H17: \u003d D13 / (D8 * 60) = 71,361
I celler D18, E18, F18, G18, H18 og den kombinerte cellen D19E19F19G19H19, er termisk kraft gitt i ARC-enheten av måling - i Gkal / time.
Denne beregningen i Excel er fullført.
Konklusjoner:
Vær oppmerksom på at det er nødvendig å bruke mer enn to ganger luften for å varme opp luften enn for oppvarming av samme masse av stål.
Når vannet er oppvarmet, er energikostnadene dobbelt så større enn når isen er oppvarmet. Smelteprosessen bruker gjentatte ganger energi enn oppvarmingsprosessen (med en liten temperaturforskjell).
Vannoppvarming ti ganger bruker mer termisk energi enn ståloppvarming og fire ganger mer enn luftoppvarming.
Til kvittering informasjon om utgivelsen av nye artikler og for last ned programarbeidsfiler vennligst abonner på kunngjøringene i vinduet som ligger på slutten av artikkelen eller øverst på siden.
Etter at du har skrevet inn adressen til e-posten din og klikker på "Motta kunngjøring" -knappen IKKE GLEMBekrefte Abonnement Klikk på linken i et brev, som umiddelbart kommer til deg på den angitte e-posten (noen ganger i mappen « Spam » )!
Vi husket konseptene "mengden varme" og "termisk kraft", betraktet som de grunnleggende formler av varmeoverføring, demontert et praktisk eksempel. Jeg håper tungen min var enkel, forståelig og interessant.
Venter på spørsmål og kommentarer til artikkelen!
spørre Respektfull arbeid forfatter Last ned fil Etter abonnement på kunngjøringer av artikler.





